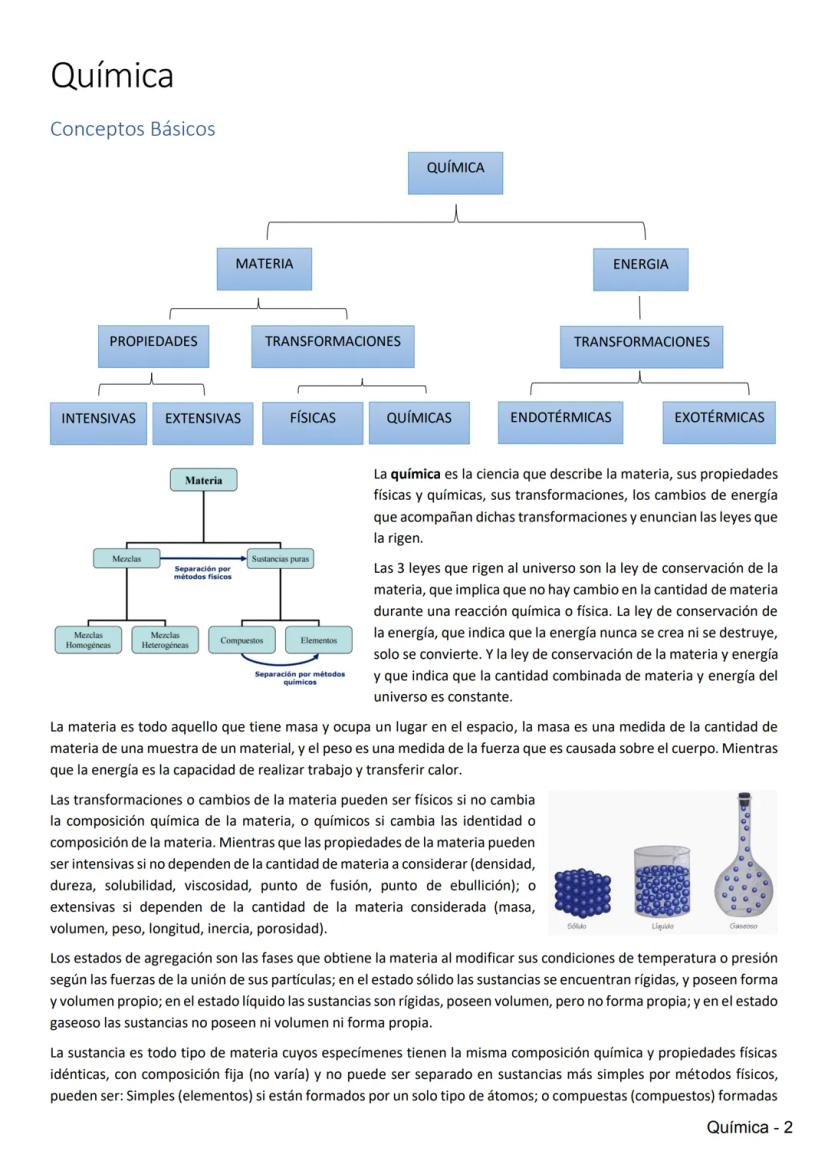
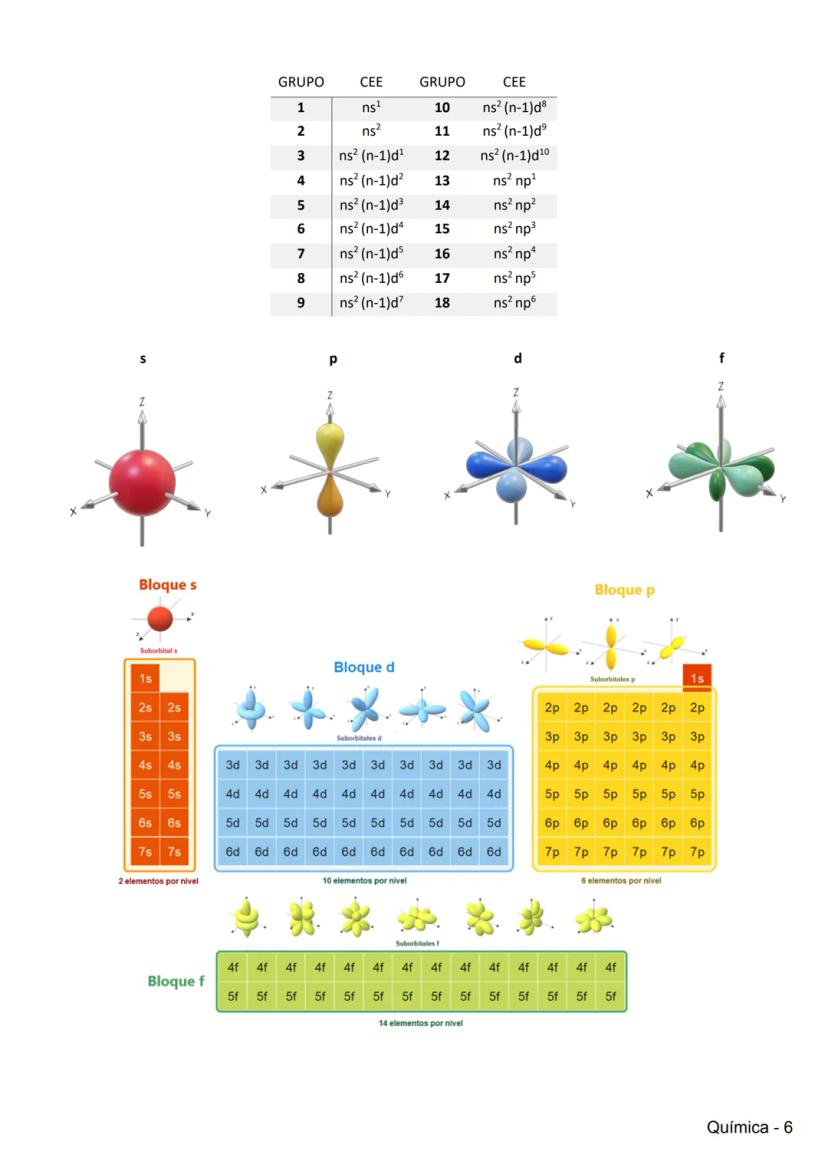
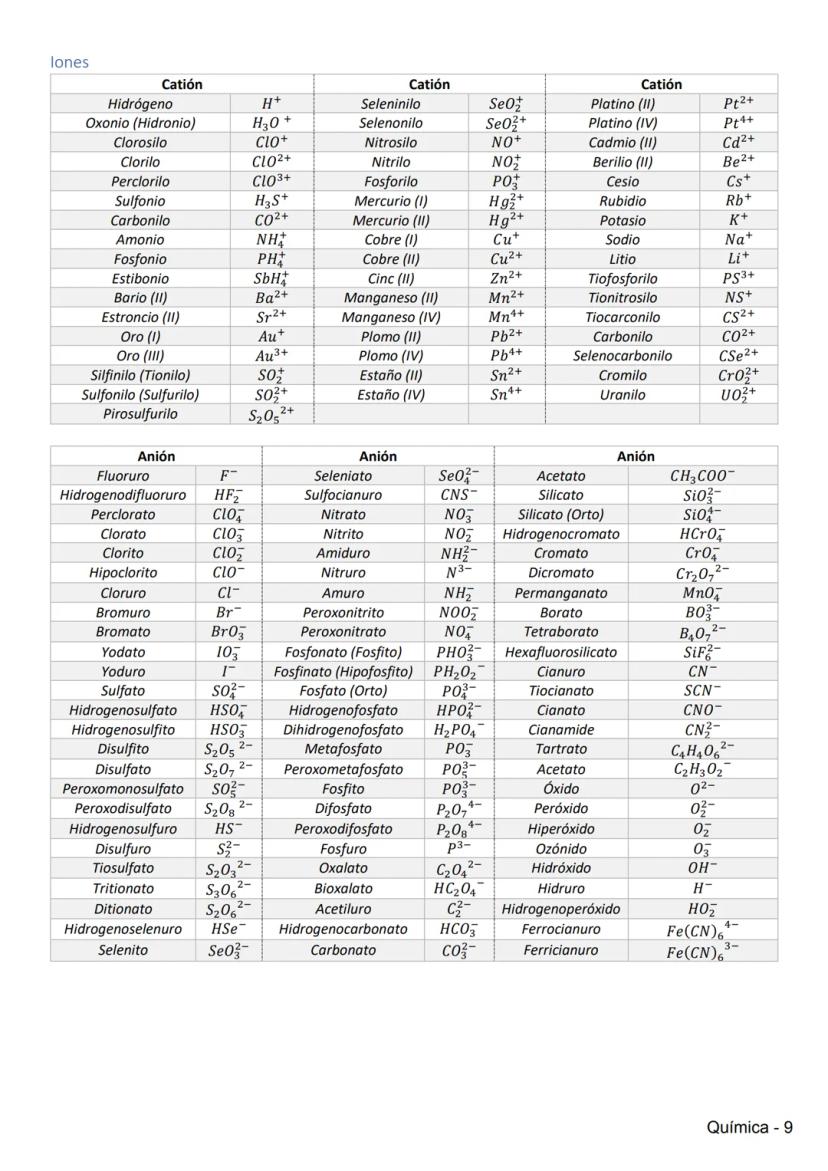
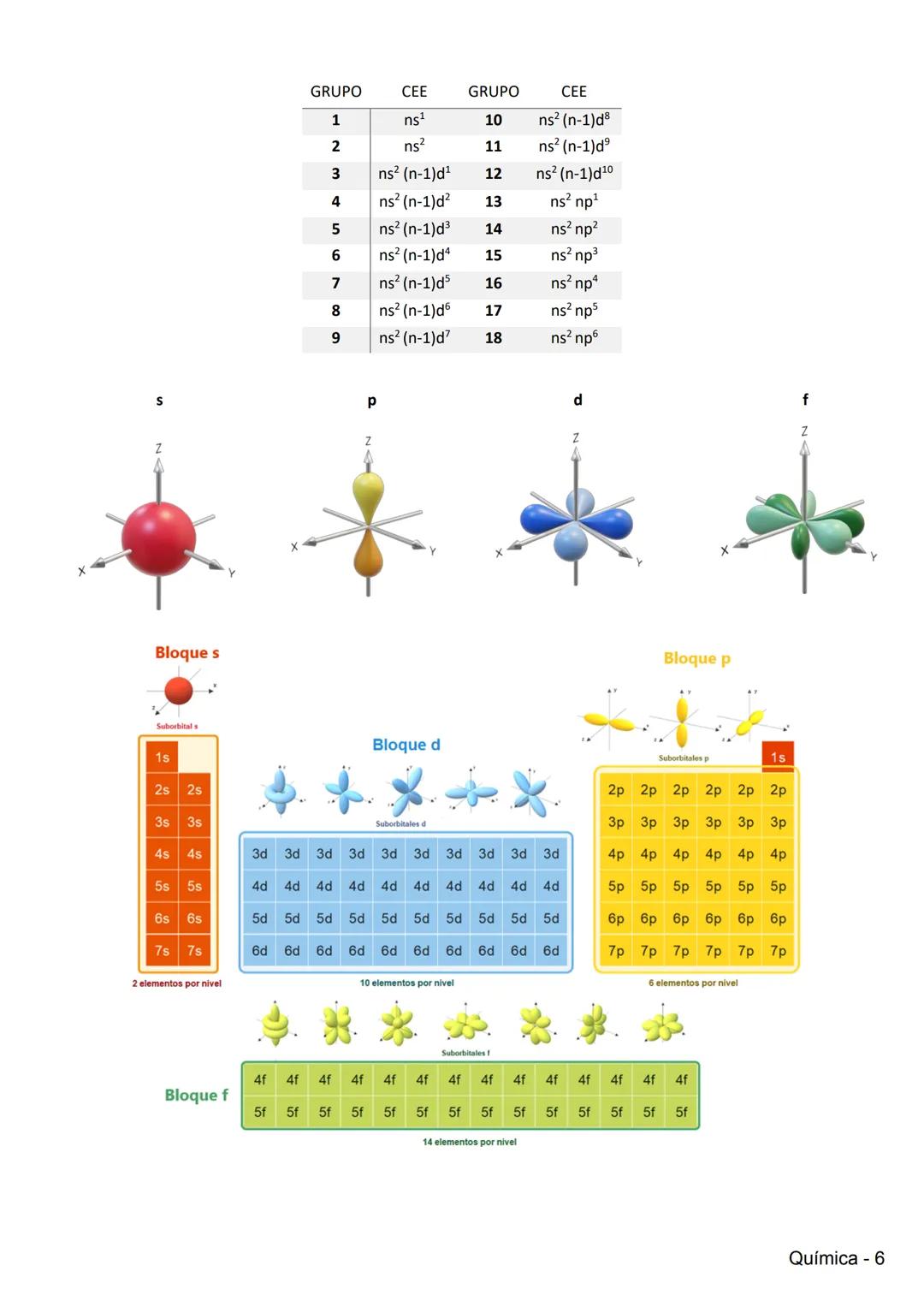
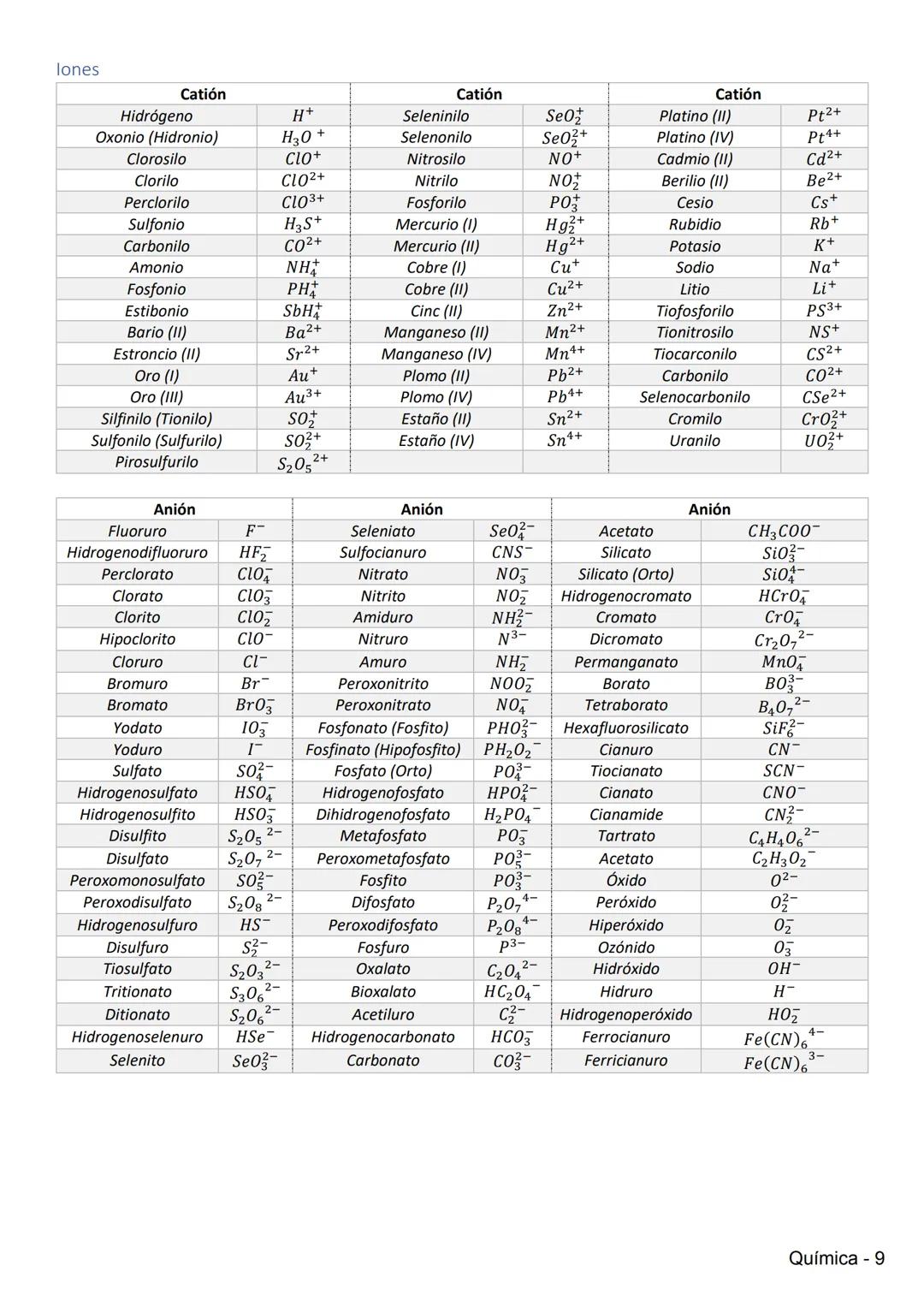
Propiedades Periódicas
La tabla periódica organiza los elementos según sus propiedades, que varían de manera predecible. Estas variaciones se deben principalmente al efecto apantallamiento (electrones internos "bloqueando" la atracción nuclear) y a la carga nuclear efectiva (atracción real que sienten los electrones externos).
Radio atómico: Disminuye de izquierda a derecha en un período (mayor carga nuclear efectiva) y aumenta de arriba hacia abajo en un grupo (nuevos niveles energéticos).
Energía de ionización: Es la energía necesaria para arrancar un electrón de un átomo. Aumenta de izquierda a derecha en un período y disminuye de arriba hacia abajo en un grupo. Elementos con alta energía de ionización son menos reactivos como metales.
⚡ Cuanto más difícil sea quitarle electrones a un átomo (alta energía de ionización), menor será su carácter metálico y mayor será su estabilidad.
Carácter metálico: Relacionado con la tendencia a ceder electrones. Aumenta de arriba hacia abajo en un grupo y de derecha a izquierda en un período. Los metales más reactivos se encuentran en la esquina inferior izquierda de la tabla.
Afinidad electrónica: Mide la tendencia a ganar electrones. Se hace más negativa de izquierda a derecha en un período y disminuye de arriba hacia abajo en un grupo.
Electronegatividad: Mide la capacidad de un átomo para atraer electrones en un enlace. Aumenta de izquierda a derecha y de abajo hacia arriba, siendo el flúor el elemento más electronegativo (valor 4 en la escala de Pauling).