Puentes de Hidrógeno y Propiedades de Líquidos
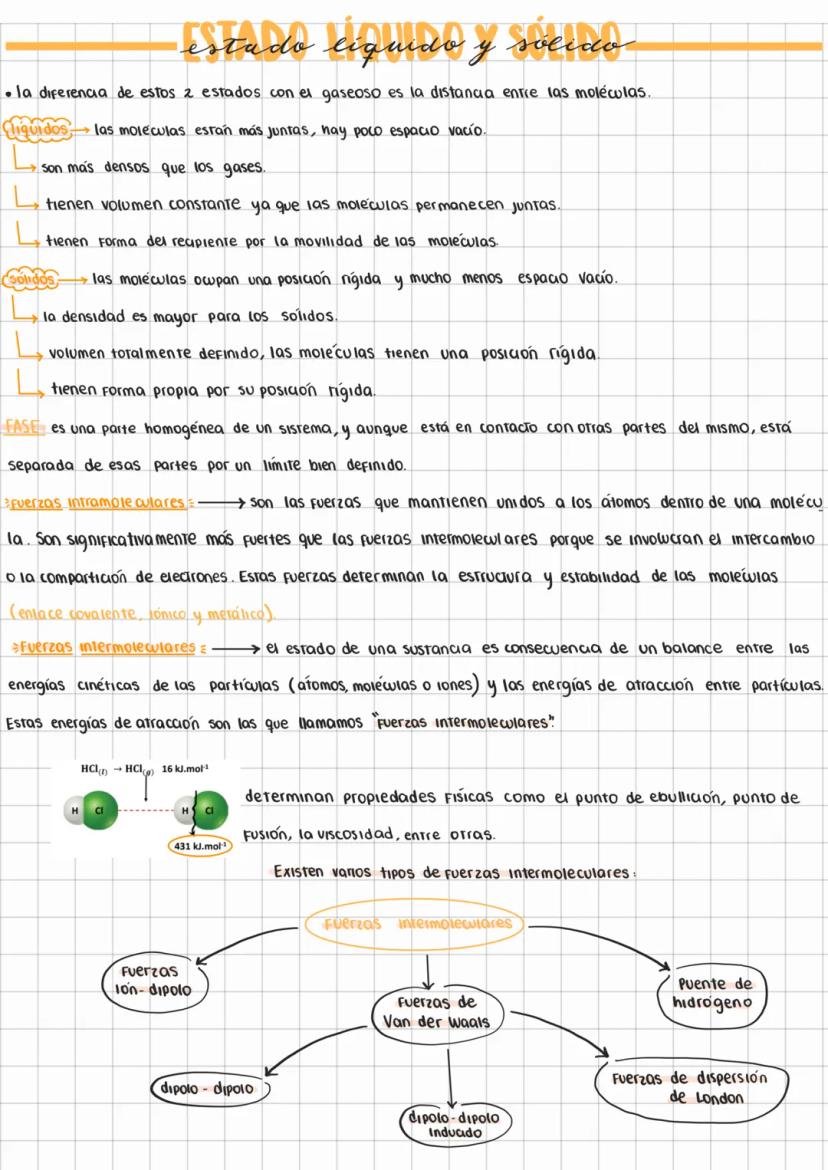
Los puentes de hidrógeno son las fuerzas intermoleculares más fuertes (después del enlace iónico). Se forman cuando un hidrógeno unido a N, O o F interactúa con otro átomo electronegativo. Por eso el agua tiene propiedades tan especiales.
La tensión superficial hace que la superficie del agua actúe como una "película elástica". Las moléculas de la superficie solo tienen vecinas hacia abajo y a los lados, no hacia arriba, creando esa resistencia que permite que algunos insectos caminen sobre el agua.
La acción capilar explica por qué los líquidos suben o bajan en tubos estrechos. Depende del balance entre adhesión (atracción al tubo) y cohesión (atracción entre moléculas del líquido). Si gana la adhesión, el líquido sube; si gana la cohesión, baja.
La viscosidad mide qué tan difícil es que un líquido fluya. La miel es más viscosa que el agua porque sus moléculas tienen fuerzas intermoleculares más fuertes. Con más temperatura, la viscosidad disminuye porque las moléculas se mueven más.
💡 Para recordar: La presión de vapor es la presión que ejerce el vapor de un líquido sobre sí mismo. Un líquido hierve cuando su presión de vapor iguala la presión externa.