Las fuerzas intermoleculares son atracciones que existen entre moléculas y... Mostrar más
Fuerzas Intermoleculares: Tipos e Importancia








Atracción Intermolecular
La atracción intermolecular representa las fuerzas que mantienen unidas a las moléculas entre sí. Estas fuerzas son fundamentales para entender por qué algunas sustancias son líquidas a temperatura ambiente mientras otras son gaseosas.
Son estas atracciones las que debes vencer cuando calientas agua para que hierva o cuando un perfume se evapora en el aire. Mientras más fuertes sean estas fuerzas, más energía necesitarás para separar las moléculas.
⚠️ ¡Dato importante! No confundas las fuerzas intermoleculares (entre moléculas) con los enlaces químicos (dentro de una misma molécula). Los enlaces son mucho más fuertes y determinan las propiedades químicas.

Bases de la Atracción Molecular
La estructura de los átomos determina cómo se forman las moléculas y, a su vez, esto influye en cómo interactúan entre ellas. Las distintas estructuras moleculares producen diferentes fuerzas de atracción entre las moléculas.
Estas fuerzas de atracción, conocidas como fuerzas de Van der Waals, varían en intensidad. Algunas mantienen a las moléculas fuertemente unidas, mientras que otras permiten que se separen con facilidad.
Las propiedades características de las sustancias, como si son sólidas, líquidas o gaseosas a temperatura ambiente, dependen directamente de la intensidad de estas fuerzas intermoleculares.

Fuerzas Intra e Intermoleculares
Las fuerzas intramoleculares son las que mantienen unidos a los átomos dentro de una molécula (uniones iónicas, metálicas o covalentes). Estas fuerzas son las que se rompen durante los cambios químicos y determinan las propiedades químicas de las sustancias.
Por otro lado, las fuerzas intermoleculares actúan entre distintas moléculas o iones, provocando atracción o repulsión. Son estas fuerzas las responsables de las propiedades físicas como el estado de agregación, puntos de fusión y ebullición, solubilidad o densidad.
Cuando calentás un hielo hasta derretirlo, no estás rompiendo los enlaces dentro de las moléculas de agua, sino venciendo las fuerzas entre ellas.
💡 ¡Entendelo así! Si pensás en una clase, los enlaces intramoleculares serían como la amistad entre dos compañeros inseparables, mientras que las fuerzas intermoleculares serían como la relación entre diferentes grupos de amigos en el aula.
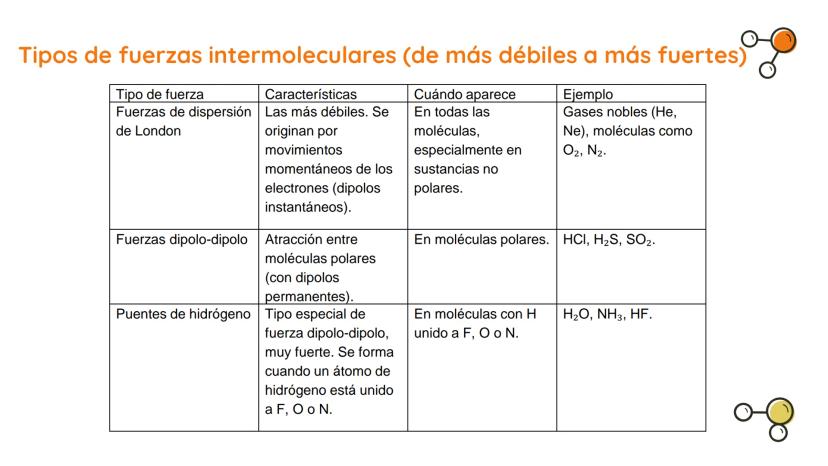
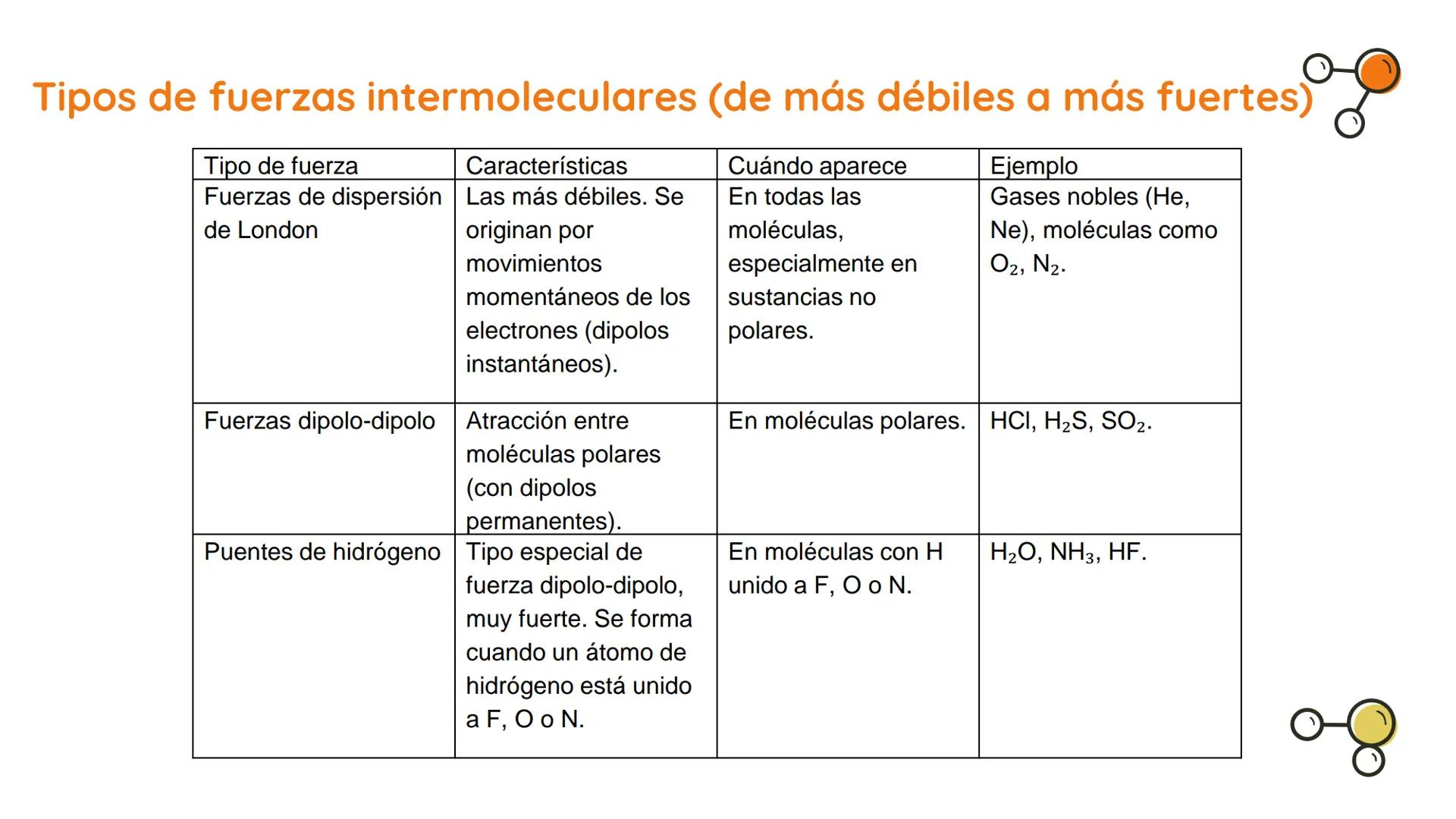
Tipos de Fuerzas de Van der Waals
Las fuerzas de Van der Waals incluyen varios tipos de interacciones moleculares que varían en intensidad. Estas fuerzas determinan cómo interactúan las moléculas entre sí.
Entre las principales podemos mencionar: fuerzas de London, interacciones dipolo-dipolo, atracciones dipolo-dipolo inducido y uniones puente de hidrógeno.
Cada tipo de fuerza actúa en situaciones específicas dependiendo de las características de las moléculas involucradas.
Fuerzas de London
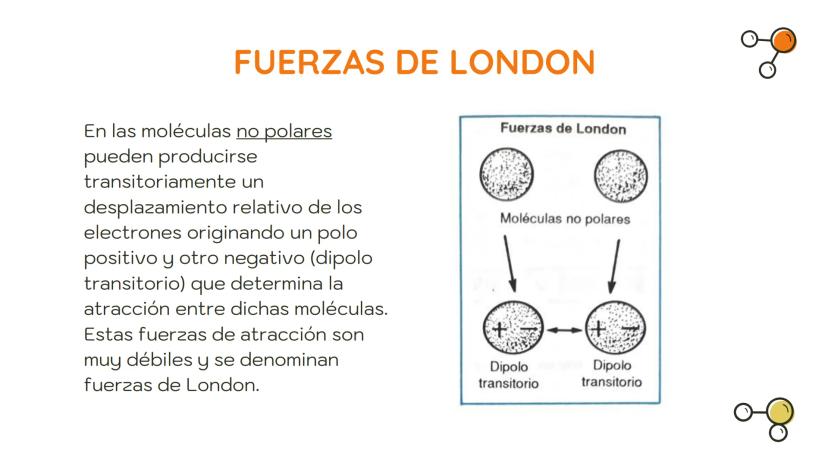
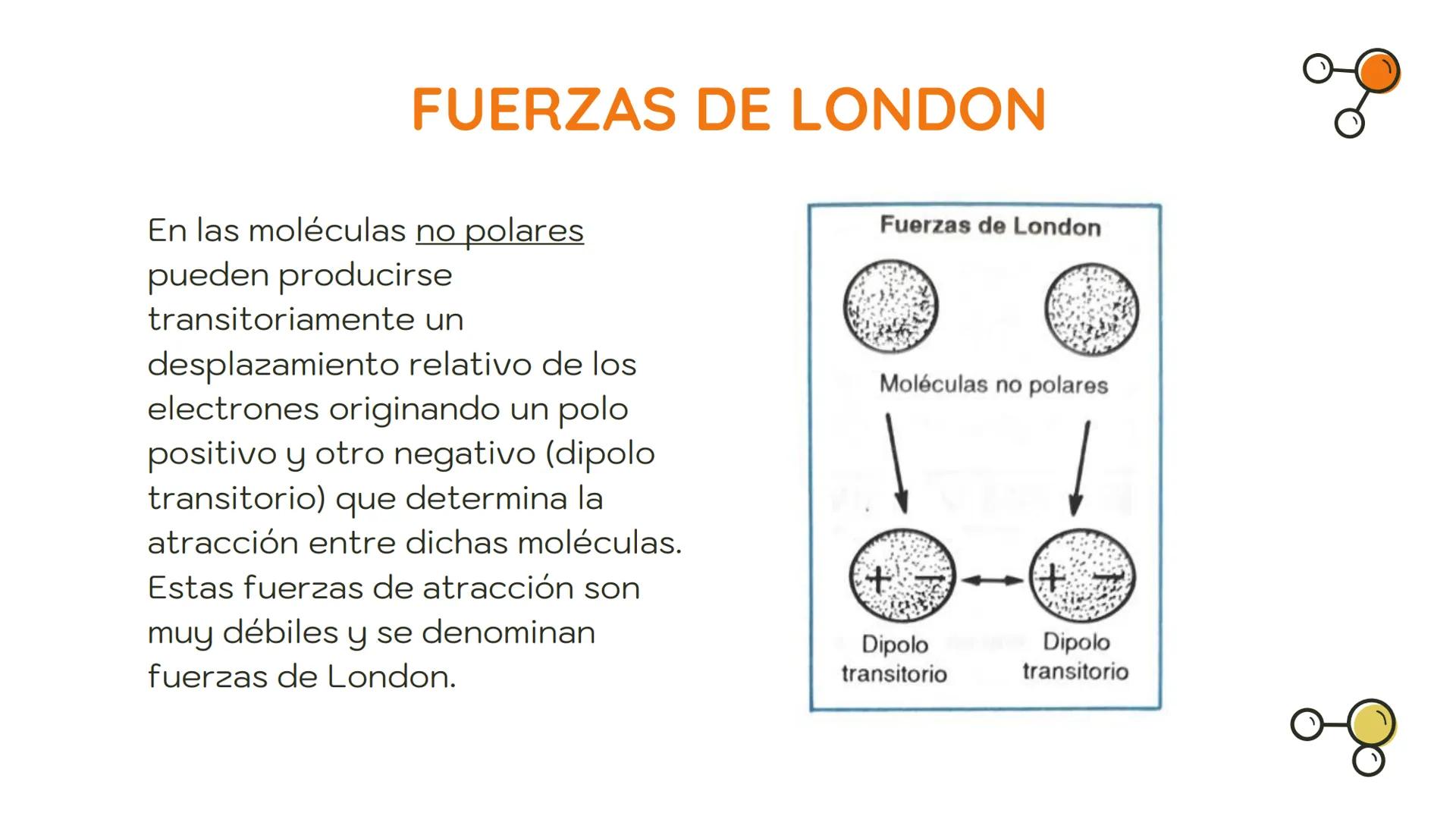
Las fuerzas de London son las más débiles de todas las interacciones intermoleculares y ocurren incluso en moléculas no polares, como el oxígeno (O₂) o el nitrógeno (N₂).
Estas fuerzas se producen cuando los electrones de una molécula no polar se desplazan momentáneamente, creando un dipolo transitorio (una separación temporal de cargas). Este dipolo momentáneo puede inducir otro dipolo en una molécula vecina, generando una atracción débil entre ambas.
Aunque son las más débiles, están presentes en todas las moléculas y son las únicas fuerzas intermoleculares en sustancias completamente no polares como los gases nobles.
🔍 ¡Visualízalo! Es como cuando dos personas que normalmente son neutrales se cargan de electricidad estática al rozar sus pies contra una alfombra, creando una atracción temporal.
Fuerzas Dipolo-Dipolo Inducido
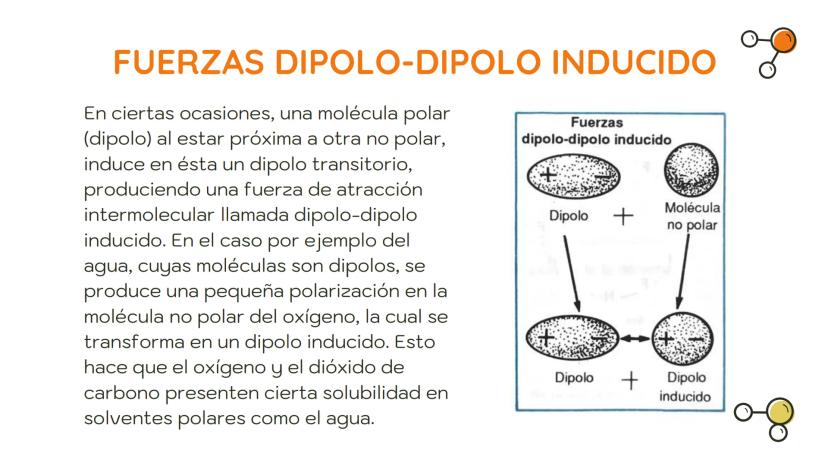
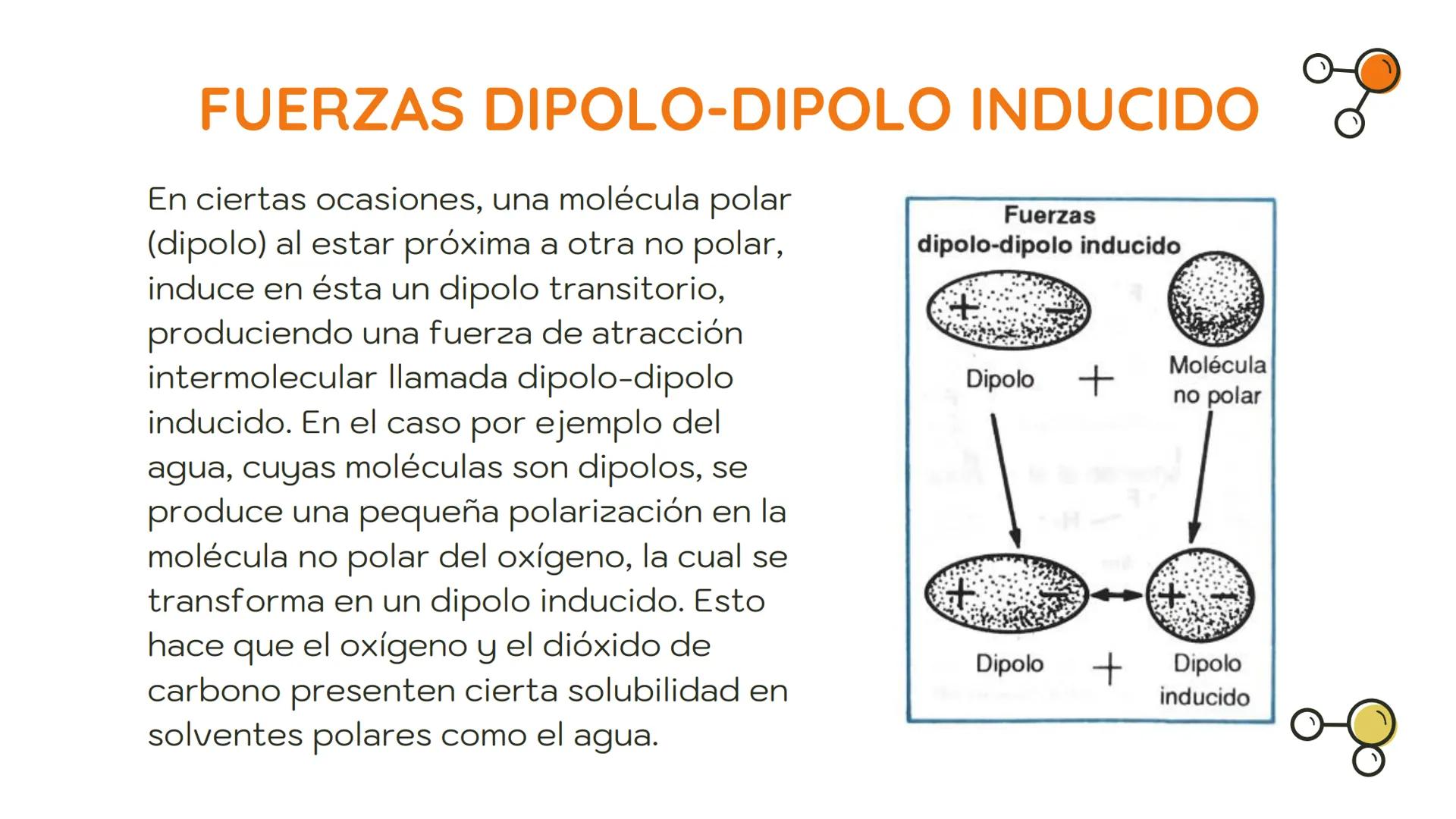
Las fuerzas dipolo-dipolo inducido ocurren cuando una molécula polar se acerca a otra no polar. La carga de la molécula polar "induce" o crea un dipolo temporal en la molécula no polar.
Por ejemplo, cuando el agua (polar) interactúa con moléculas de oxígeno (no polar), la polaridad del agua provoca una pequeña distorsión en la distribución de electrones del oxígeno, creando un dipolo inducido.
Esta interacción explica por qué gases como el oxígeno y el dióxido de carbono, aunque son no polares, pueden disolverse parcialmente en agua. Esta solubilidad es fundamental para la vida acuática y para nuestra respiración.
🧪 ¡Aplicación práctica! Gracias a estas fuerzas, los peces pueden obtener el oxígeno disuelto en el agua para sobrevivir, y nuestros pulmones pueden captar el oxígeno del aire.
Fuerzas Dipolo-Dipolo
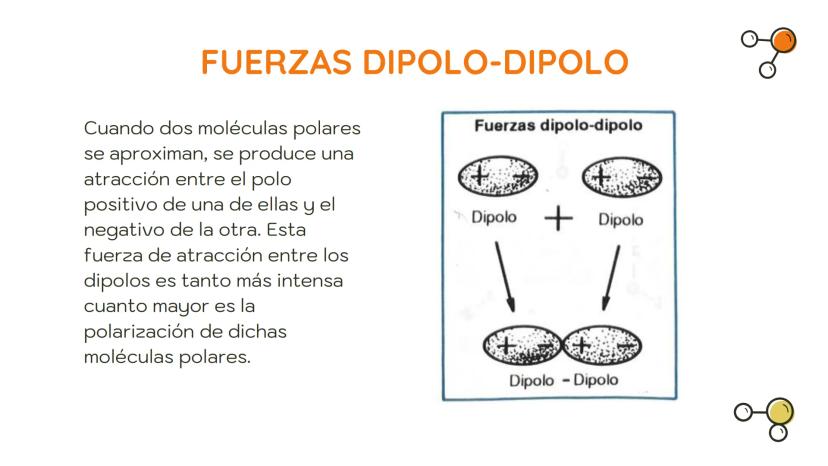
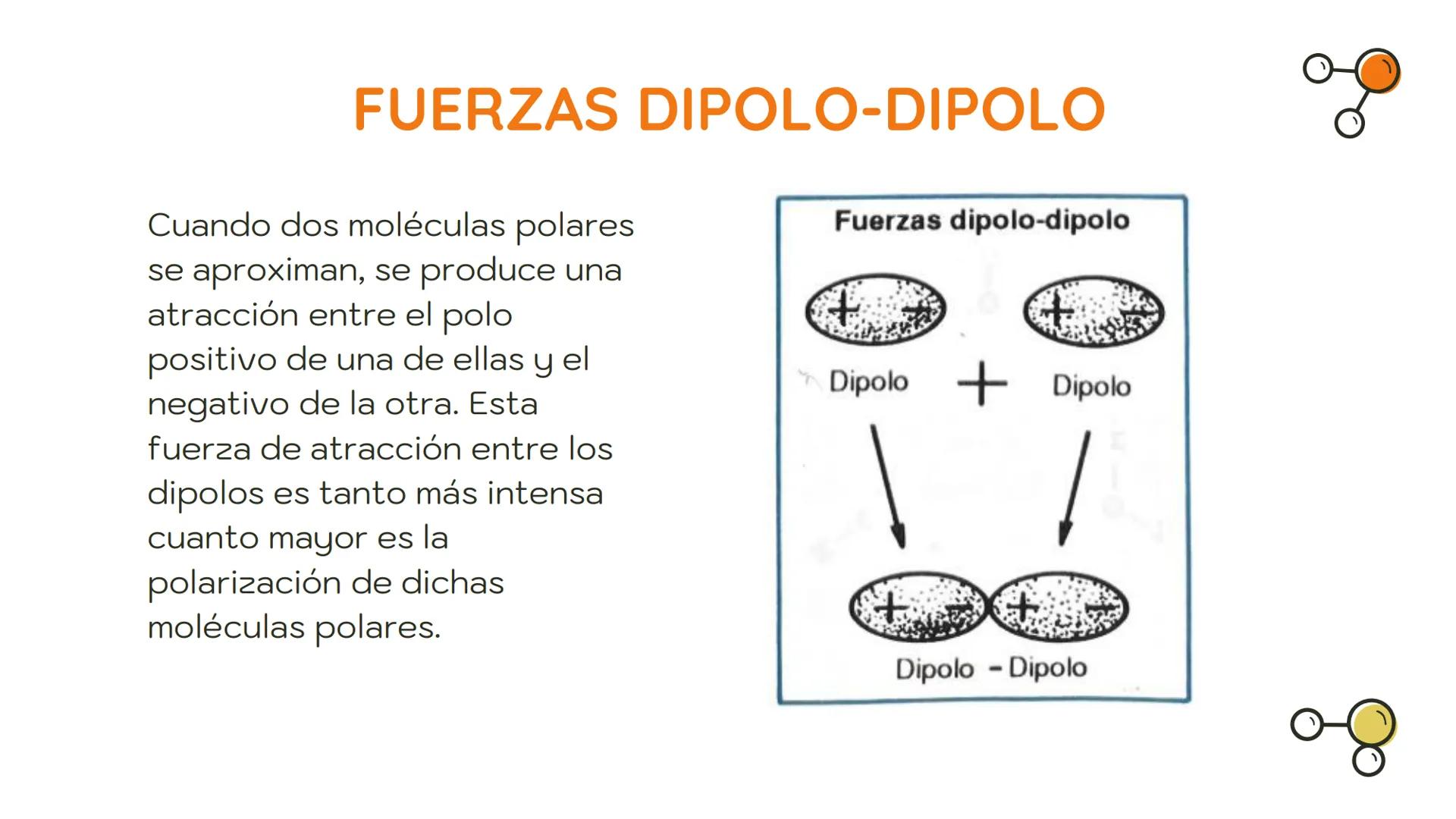
Las fuerzas dipolo-dipolo se producen entre moléculas que tienen dipolos permanentes, es decir, que son naturalmente polares. En estas moléculas, los electrones están distribuidos de forma desigual, creando una región con carga parcial positiva y otra con carga parcial negativa.
Cuando dos de estas moléculas polares se aproximan, el polo positivo de una se siente atraído por el polo negativo de la otra. Esta atracción mantiene a las moléculas unidas con una fuerza mayor que las de London.
La intensidad de estas fuerzas depende directamente del grado de polaridad de las moléculas: cuanto más polarizadas estén, más fuerte será la atracción entre ellas.
💡 ¡Pensalo así! Es como dos imanes pequeños que se atraen cuando acercás el polo norte de uno al polo sur del otro.
Unión Puente de Hidrógeno
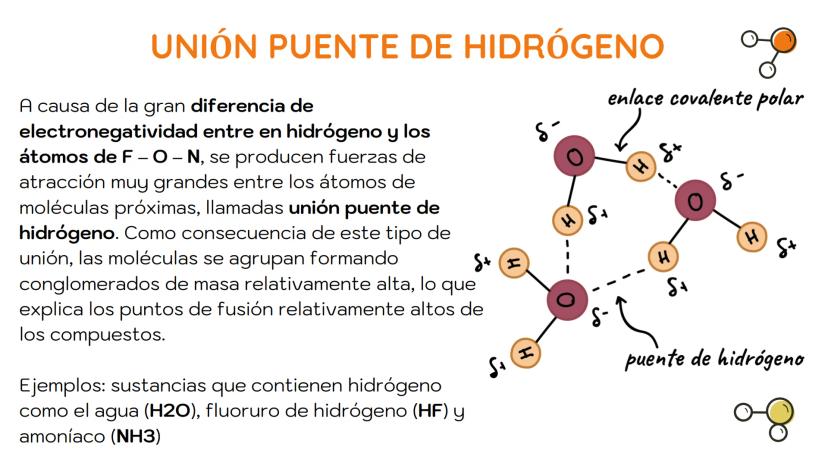
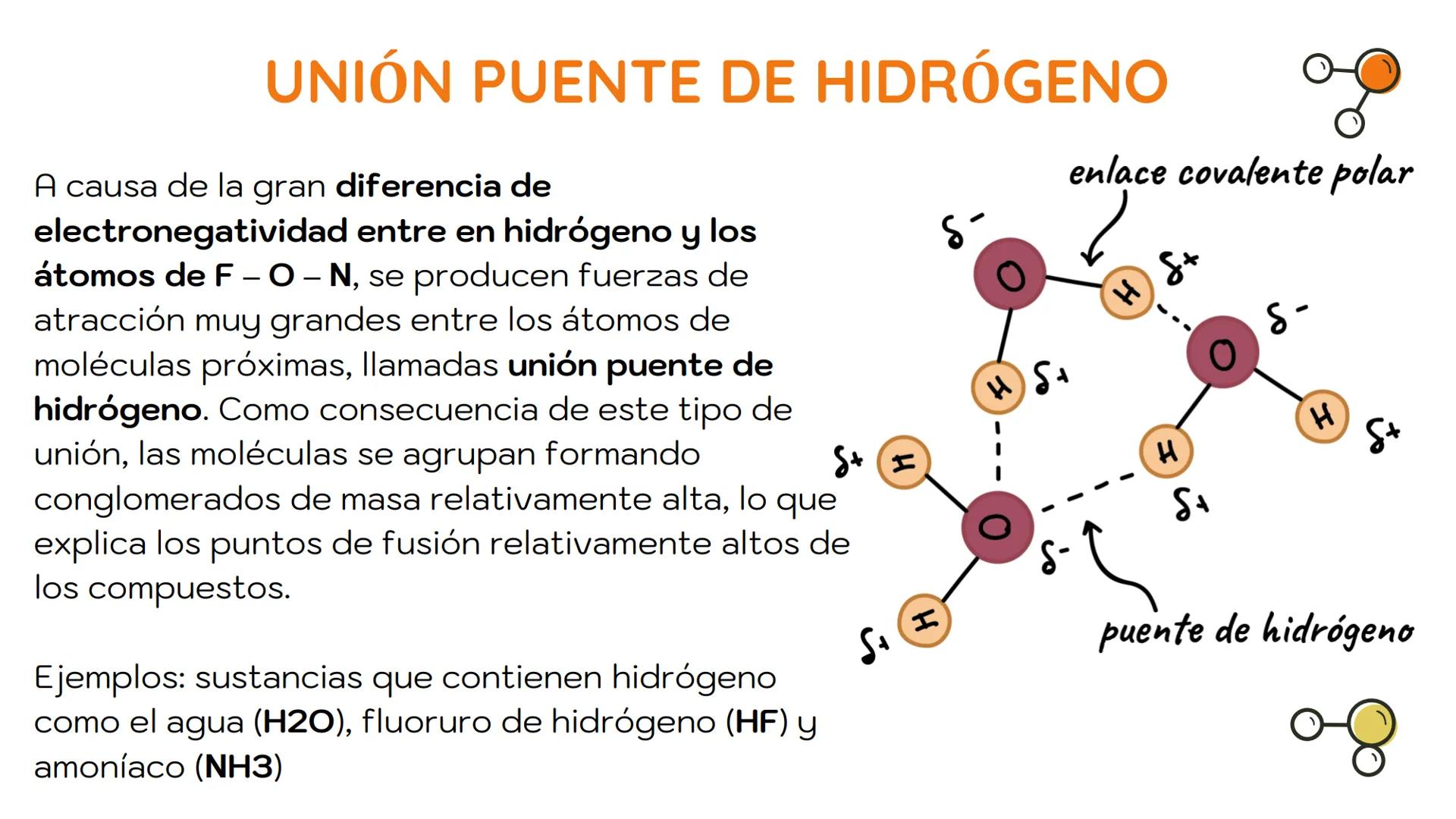
La unión puente de hidrógeno es un tipo especial de fuerza dipolo-dipolo particularmente fuerte. Se produce cuando un átomo de hidrógeno está unido covalentemente a átomos muy electronegativos como flúor (F), oxígeno (O) o nitrógeno (N).
Debido a la gran diferencia de electronegatividad, el hidrógeno queda con una fuerte carga parcial positiva que es atraída por los pares de electrones libres de átomos F, O o N de moléculas vecinas.
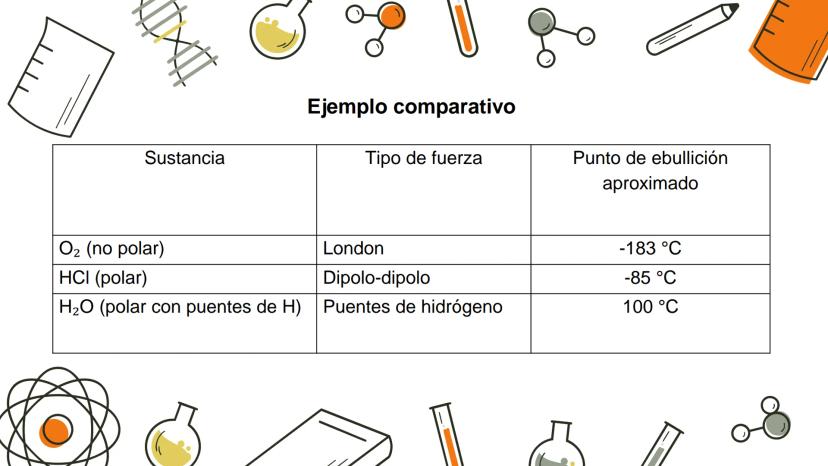
Esta unión es responsable de propiedades peculiares como los altos puntos de fusión y ebullición del agua (H₂O), fluoruro de hidrógeno (HF) y amoníaco (NH₃). Las moléculas se agrupan formando "conglomerados" que requieren mucha energía para separarse.
🔥 ¡Increíble pero cierto! Si el agua no formara puentes de hidrógeno, herviría a aproximadamente -80°C en lugar de 100°C, y la vida como la conocemos sería imposible.
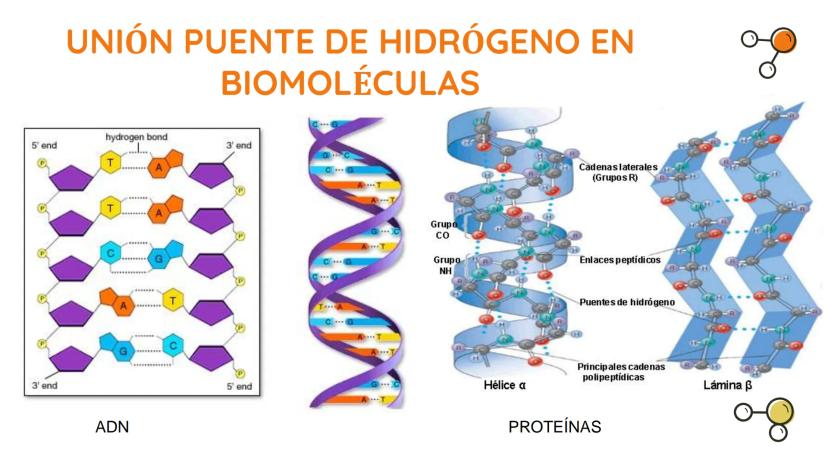
Unión Puente de Hidrógeno en Biomoléculas
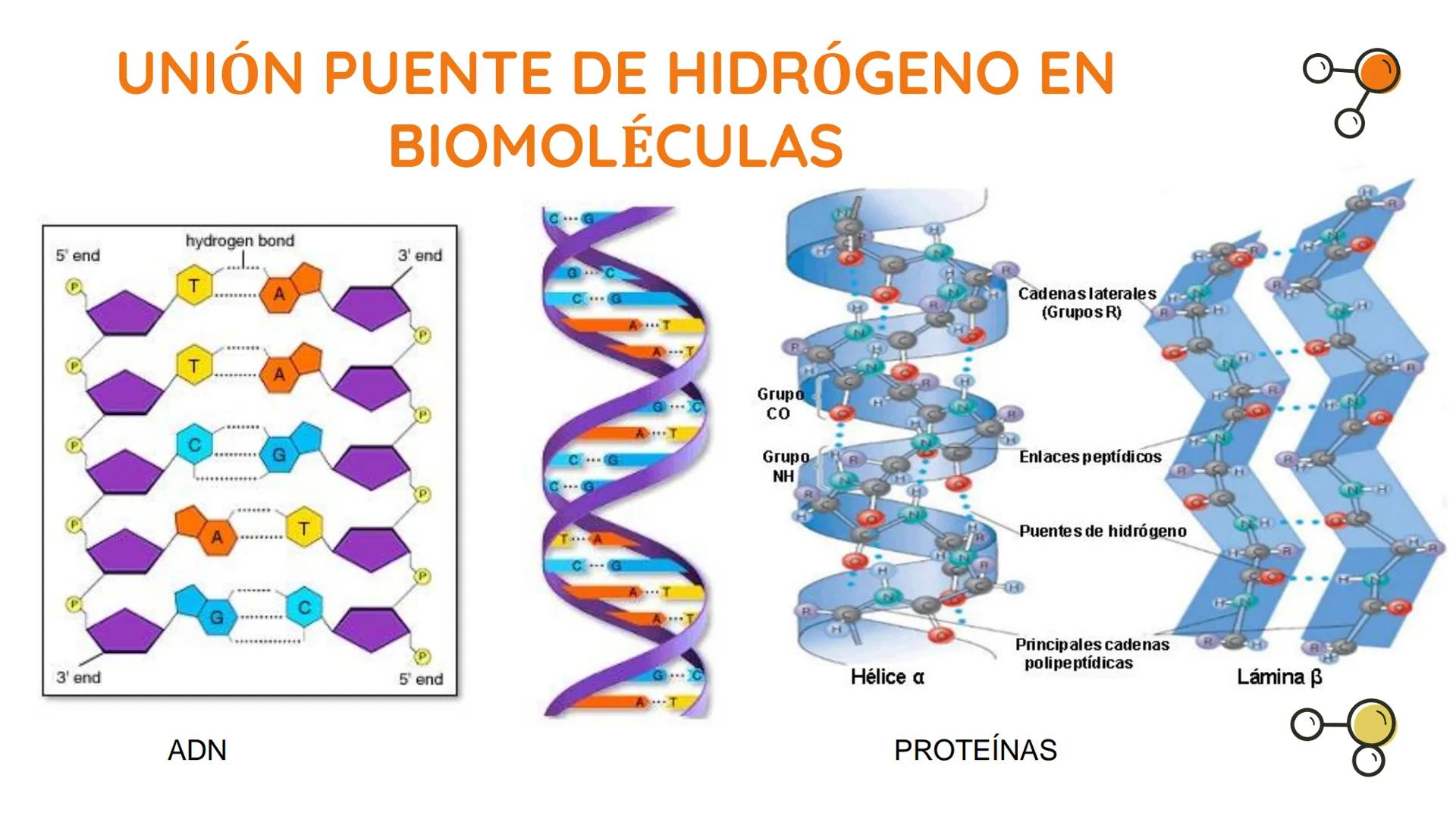
Los puentes de hidrógeno juegan un papel fundamental en la estructura y función de las biomoléculas, siendo esenciales para la vida.
En el ADN, los puentes de hidrógeno mantienen unidas las dos hebras de la famosa doble hélice. Estas uniones se forman específicamente entre bases complementarias , permitiendo que la información genética se copie fielmente durante la replicación.
En las proteínas, los puentes de hidrógeno determinan su estructura tridimensional. Forman y estabilizan las estructuras secundarias como la hélice α y la lámina β, que son fundamentales para la función biológica de las proteínas.
🧬 ¡Fascinante! Sin los puentes de hidrógeno, tu ADN se "desarmaría" como una cremallera y las proteínas perderían su forma funcional, haciendo imposible la vida tal como la conocemos.

Resumen de Fuerzas Intermoleculares
Las fuerzas intermoleculares son atracciones que existen entre moléculas, no dentro de ellas. Aunque son más débiles que los enlaces químicos, su importancia es enorme para entender el mundo que nos rodea.
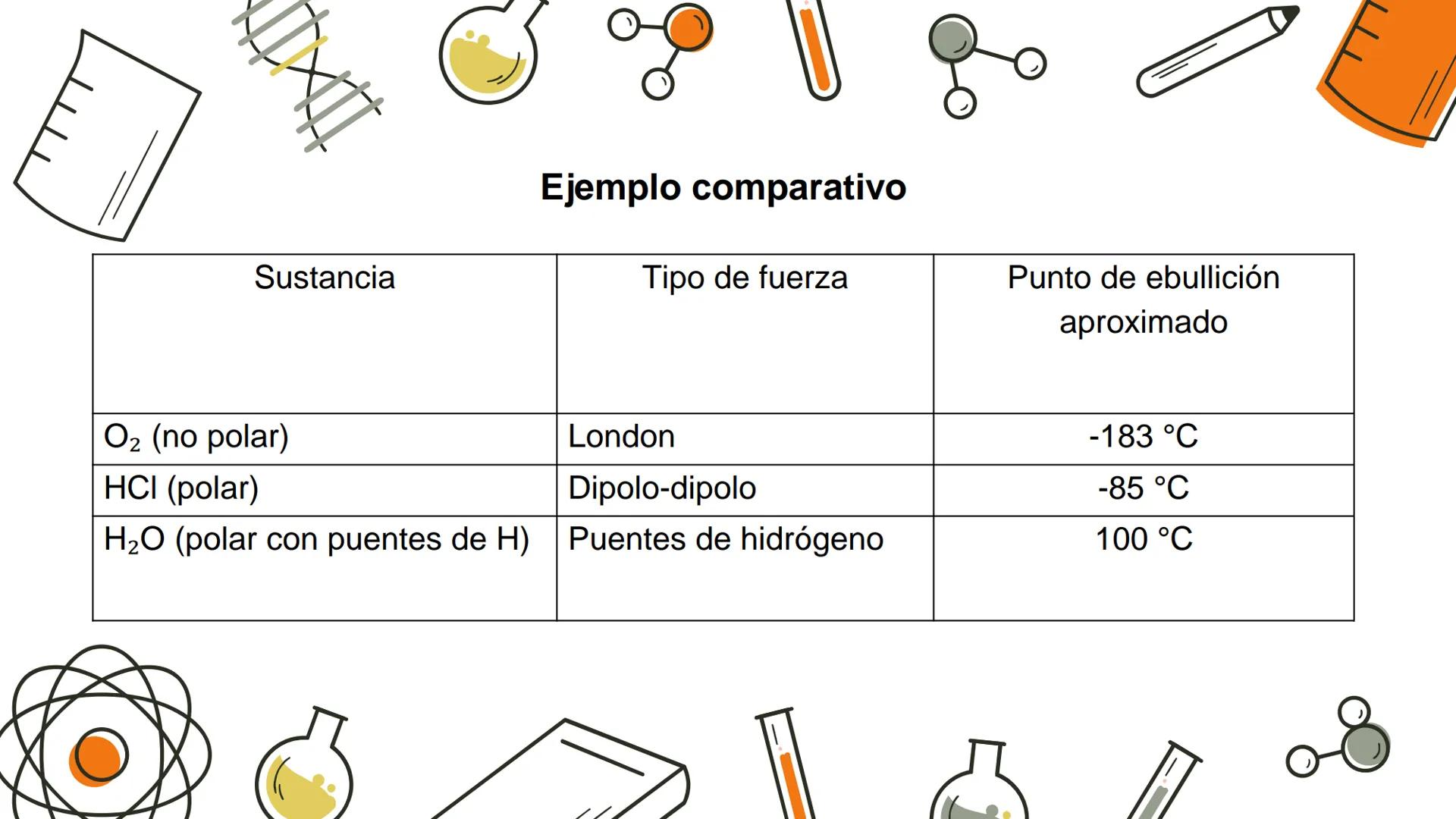
Estas fuerzas influyen directamente en propiedades físicas como el punto de ebullición, punto de fusión, viscosidad y solubilidad de las sustancias. Por ejemplo, determinan si una sustancia será un gas, un líquido o un sólido a temperatura ambiente.
La próxima vez que tomes agua, pensá en los puentes de hidrógeno que mantienen unidas sus moléculas. Sin estas fuerzas, el agua sería un gas a temperatura ambiente y la vida en la Tierra sería imposible tal como la conocemos.



Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares: Properties of Matter
9Enlaces químicos
Clasificación de enlaces intermoleculares e intramoleculares
Uniones quimicas
.
materia,cuerpo y sustancia
resubi las actividades del final respecto a los textos
quimica inorganica. Formulas Quimicas. Nomenclatura
Apuntes del profesor de la asignatura de Quimica de ultimo año de secundaria!tema: Quimica inorganica. Formulas Quimicas. Nomenclatura, Quimica organica
Métodos de análisis químicos
Química Aplicada
Lipidos
.
La materia y sistemas materiales
Con esto tuve nota 10 así que ahí les va
Materia y sus propiedades
Esta lección introduce el concepto de materia, definiéndola como todo lo que ocupa espacio y tiene masa, y explica sus propiedades fundamentales de volumen y masa.
Teoría cinetico corpuscular
Apunte sobre como se describe la materia y sus características.
Contenidos más populares de Química
9Enlaces químicos
Clasificación de enlaces intermoleculares e intramoleculares
Metabolismo
Metabolismo
Apunte de Hidratos de Carbono
Este apunte profundiza de forma clara y estructurada en el mundo de los glúcidos, desde la clasificación de los monosacáridos hasta la complejidad de los gluconjugados. Ideal para estudiantes que buscan entender su estructura, función y reactividad.
Ácidos Nucleicos & Genética Molecular: La Ruta Completa del ADN a las Proteínas
Este apunte desglosa con claridad y profundidad la estructura y función de los ácidos nucleicos, brindando una guía completa desde los nucleótidos hasta el código genético y la síntesis proteica.
Materia
Necesito un rsusmen de esta unidad con lo mas imoortante para rendir en diciembre
Apunte de Proteínas; Aminoácidos y Enzimas
Este apunte te lleva paso a paso por los pilares de la bioquímica proteica. Desde la estructura de los aminoácidos hasta las enzimas, pasando por niveles estructurales, clasificación funcional y patologías asociadas.
estados de transformaciones de la materia
resumen
Apunte de Lípidos; Estrutura química y función
Este apunte explora en profundidad la bioquímica de los lípidos, desde los ácidos grasos esenciales hasta esteroides y lipoproteínas. Organizado de forma clara y visual, presenta cada categoría con sus estructuras, funciones y ejemplos clínicos.
Quimica organica
Guia con ejercicios quimica
Contenidos más populares
9Biologia
Fases
Conceptos Clave de la Revolución Industrial
Explora los términos esenciales de la Revolución Industrial, sus clases sociales y la urbanización.
Países y Capitales de América
Aprende los países y capitales de América del Sur, Central, Caribe y del Norte.
matematicas
ecuaciones
celula eucriota, membrana plasmática, núcleo, pared celular, citoplasma y citoesqueletos. nombre se las partes de la celula eucariota
Este quiz evalúa tu conocimiento sobre la célula eucariota, incluyendo la membrana plasmática, núcleo, pared celular, citoplasma y citoesqueleto.
Precalculo
Estoy estudiando temas de Álgebra y Trigonometría (logaritmos, funciones cuadráticas, identidades trigonométricas) y Física (vectores, cinemática, estática). Mi objetivo es aprobar el examen de ingreso a Ingeniería Industrial.
Análisis sintáctico de oraciones
explicación de el análisis de oraciones
Función cuadrática: Fórmulas y Análisis de la parábola.
Resumen teórico-práctico sobre la función cuadrática, sus fórmulas principales y el estudio de la parábola como representación gráfica.Incluye desarrollo de la forma general, cálculo de raíces, vértice y elementos fundamentales para su interpretación
Geografía 1er año
definición geografía-coordenadas geográficas-meridianos-paralelos-definición latitud y longitud-elementos del mapa-definición mapa-localización relativa y absoluta
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encantó — y a ti también te encantará.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Fuerzas Intermoleculares: Tipos e Importancia
Las fuerzas intermoleculares son atracciones que existen entre moléculas y determinan las propiedades físicas de las sustancias. Aunque son más débiles que los enlaces químicos, estas fuerzas influyen directamente en características como los puntos de fusión y ebullición, la solubilidad... Mostrar más

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Atracción Intermolecular
La atracción intermolecular representa las fuerzas que mantienen unidas a las moléculas entre sí. Estas fuerzas son fundamentales para entender por qué algunas sustancias son líquidas a temperatura ambiente mientras otras son gaseosas.
Son estas atracciones las que debes vencer cuando calientas agua para que hierva o cuando un perfume se evapora en el aire. Mientras más fuertes sean estas fuerzas, más energía necesitarás para separar las moléculas.
⚠️ ¡Dato importante! No confundas las fuerzas intermoleculares (entre moléculas) con los enlaces químicos (dentro de una misma molécula). Los enlaces son mucho más fuertes y determinan las propiedades químicas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Bases de la Atracción Molecular
La estructura de los átomos determina cómo se forman las moléculas y, a su vez, esto influye en cómo interactúan entre ellas. Las distintas estructuras moleculares producen diferentes fuerzas de atracción entre las moléculas.
Estas fuerzas de atracción, conocidas como fuerzas de Van der Waals, varían en intensidad. Algunas mantienen a las moléculas fuertemente unidas, mientras que otras permiten que se separen con facilidad.
Las propiedades características de las sustancias, como si son sólidas, líquidas o gaseosas a temperatura ambiente, dependen directamente de la intensidad de estas fuerzas intermoleculares.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas Intra e Intermoleculares
Las fuerzas intramoleculares son las que mantienen unidos a los átomos dentro de una molécula (uniones iónicas, metálicas o covalentes). Estas fuerzas son las que se rompen durante los cambios químicos y determinan las propiedades químicas de las sustancias.
Por otro lado, las fuerzas intermoleculares actúan entre distintas moléculas o iones, provocando atracción o repulsión. Son estas fuerzas las responsables de las propiedades físicas como el estado de agregación, puntos de fusión y ebullición, solubilidad o densidad.
Cuando calentás un hielo hasta derretirlo, no estás rompiendo los enlaces dentro de las moléculas de agua, sino venciendo las fuerzas entre ellas.
💡 ¡Entendelo así! Si pensás en una clase, los enlaces intramoleculares serían como la amistad entre dos compañeros inseparables, mientras que las fuerzas intermoleculares serían como la relación entre diferentes grupos de amigos en el aula.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Tipos de Fuerzas de Van der Waals
Las fuerzas de Van der Waals incluyen varios tipos de interacciones moleculares que varían en intensidad. Estas fuerzas determinan cómo interactúan las moléculas entre sí.
Entre las principales podemos mencionar: fuerzas de London, interacciones dipolo-dipolo, atracciones dipolo-dipolo inducido y uniones puente de hidrógeno.
Cada tipo de fuerza actúa en situaciones específicas dependiendo de las características de las moléculas involucradas.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas de London
Las fuerzas de London son las más débiles de todas las interacciones intermoleculares y ocurren incluso en moléculas no polares, como el oxígeno (O₂) o el nitrógeno (N₂).
Estas fuerzas se producen cuando los electrones de una molécula no polar se desplazan momentáneamente, creando un dipolo transitorio (una separación temporal de cargas). Este dipolo momentáneo puede inducir otro dipolo en una molécula vecina, generando una atracción débil entre ambas.
Aunque son las más débiles, están presentes en todas las moléculas y son las únicas fuerzas intermoleculares en sustancias completamente no polares como los gases nobles.
🔍 ¡Visualízalo! Es como cuando dos personas que normalmente son neutrales se cargan de electricidad estática al rozar sus pies contra una alfombra, creando una atracción temporal.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas Dipolo-Dipolo Inducido
Las fuerzas dipolo-dipolo inducido ocurren cuando una molécula polar se acerca a otra no polar. La carga de la molécula polar "induce" o crea un dipolo temporal en la molécula no polar.
Por ejemplo, cuando el agua (polar) interactúa con moléculas de oxígeno (no polar), la polaridad del agua provoca una pequeña distorsión en la distribución de electrones del oxígeno, creando un dipolo inducido.
Esta interacción explica por qué gases como el oxígeno y el dióxido de carbono, aunque son no polares, pueden disolverse parcialmente en agua. Esta solubilidad es fundamental para la vida acuática y para nuestra respiración.
🧪 ¡Aplicación práctica! Gracias a estas fuerzas, los peces pueden obtener el oxígeno disuelto en el agua para sobrevivir, y nuestros pulmones pueden captar el oxígeno del aire.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Fuerzas Dipolo-Dipolo
Las fuerzas dipolo-dipolo se producen entre moléculas que tienen dipolos permanentes, es decir, que son naturalmente polares. En estas moléculas, los electrones están distribuidos de forma desigual, creando una región con carga parcial positiva y otra con carga parcial negativa.
Cuando dos de estas moléculas polares se aproximan, el polo positivo de una se siente atraído por el polo negativo de la otra. Esta atracción mantiene a las moléculas unidas con una fuerza mayor que las de London.
La intensidad de estas fuerzas depende directamente del grado de polaridad de las moléculas: cuanto más polarizadas estén, más fuerte será la atracción entre ellas.
💡 ¡Pensalo así! Es como dos imanes pequeños que se atraen cuando acercás el polo norte de uno al polo sur del otro.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Unión Puente de Hidrógeno
La unión puente de hidrógeno es un tipo especial de fuerza dipolo-dipolo particularmente fuerte. Se produce cuando un átomo de hidrógeno está unido covalentemente a átomos muy electronegativos como flúor (F), oxígeno (O) o nitrógeno (N).
Debido a la gran diferencia de electronegatividad, el hidrógeno queda con una fuerte carga parcial positiva que es atraída por los pares de electrones libres de átomos F, O o N de moléculas vecinas.
Esta unión es responsable de propiedades peculiares como los altos puntos de fusión y ebullición del agua (H₂O), fluoruro de hidrógeno (HF) y amoníaco (NH₃). Las moléculas se agrupan formando "conglomerados" que requieren mucha energía para separarse.
🔥 ¡Increíble pero cierto! Si el agua no formara puentes de hidrógeno, herviría a aproximadamente -80°C en lugar de 100°C, y la vida como la conocemos sería imposible.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Unión Puente de Hidrógeno en Biomoléculas
Los puentes de hidrógeno juegan un papel fundamental en la estructura y función de las biomoléculas, siendo esenciales para la vida.
En el ADN, los puentes de hidrógeno mantienen unidas las dos hebras de la famosa doble hélice. Estas uniones se forman específicamente entre bases complementarias , permitiendo que la información genética se copie fielmente durante la replicación.
En las proteínas, los puentes de hidrógeno determinan su estructura tridimensional. Forman y estabilizan las estructuras secundarias como la hélice α y la lámina β, que son fundamentales para la función biológica de las proteínas.
🧬 ¡Fascinante! Sin los puentes de hidrógeno, tu ADN se "desarmaría" como una cremallera y las proteínas perderían su forma funcional, haciendo imposible la vida tal como la conocemos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Resumen de Fuerzas Intermoleculares
Las fuerzas intermoleculares son atracciones que existen entre moléculas, no dentro de ellas. Aunque son más débiles que los enlaces químicos, su importancia es enorme para entender el mundo que nos rodea.
Estas fuerzas influyen directamente en propiedades físicas como el punto de ebullición, punto de fusión, viscosidad y solubilidad de las sustancias. Por ejemplo, determinan si una sustancia será un gas, un líquido o un sólido a temperatura ambiente.
La próxima vez que tomes agua, pensá en los puentes de hidrógeno que mantienen unidas sus moléculas. Sin estas fuerzas, el agua sería un gas a temperatura ambiente y la vida en la Tierra sería imposible tal como la conocemos.

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes

Inscríbete para ver los apuntes. ¡Es gratis!
- Acceso a todos los documentos
- Mejora tus notas
- Únete a millones de estudiantes
Pensamos que nunca lo preguntarías...
¿Qué es Knowunity AI companion?
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
¿Dónde puedo descargar la app Knowunity?
Puedes descargar la app en Google Play Store y Apple App Store.
¿Knowunity es totalmente gratuito?
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
Contenidos más populares: Properties of Matter
9Enlaces químicos
Clasificación de enlaces intermoleculares e intramoleculares
Uniones quimicas
.
materia,cuerpo y sustancia
resubi las actividades del final respecto a los textos
quimica inorganica. Formulas Quimicas. Nomenclatura
Apuntes del profesor de la asignatura de Quimica de ultimo año de secundaria!tema: Quimica inorganica. Formulas Quimicas. Nomenclatura, Quimica organica
Métodos de análisis químicos
Química Aplicada
Lipidos
.
La materia y sistemas materiales
Con esto tuve nota 10 así que ahí les va
Materia y sus propiedades
Esta lección introduce el concepto de materia, definiéndola como todo lo que ocupa espacio y tiene masa, y explica sus propiedades fundamentales de volumen y masa.
Teoría cinetico corpuscular
Apunte sobre como se describe la materia y sus características.
Contenidos más populares de Química
9Enlaces químicos
Clasificación de enlaces intermoleculares e intramoleculares
Metabolismo
Metabolismo
Apunte de Hidratos de Carbono
Este apunte profundiza de forma clara y estructurada en el mundo de los glúcidos, desde la clasificación de los monosacáridos hasta la complejidad de los gluconjugados. Ideal para estudiantes que buscan entender su estructura, función y reactividad.
Ácidos Nucleicos & Genética Molecular: La Ruta Completa del ADN a las Proteínas
Este apunte desglosa con claridad y profundidad la estructura y función de los ácidos nucleicos, brindando una guía completa desde los nucleótidos hasta el código genético y la síntesis proteica.
Materia
Necesito un rsusmen de esta unidad con lo mas imoortante para rendir en diciembre
Apunte de Proteínas; Aminoácidos y Enzimas
Este apunte te lleva paso a paso por los pilares de la bioquímica proteica. Desde la estructura de los aminoácidos hasta las enzimas, pasando por niveles estructurales, clasificación funcional y patologías asociadas.
estados de transformaciones de la materia
resumen
Apunte de Lípidos; Estrutura química y función
Este apunte explora en profundidad la bioquímica de los lípidos, desde los ácidos grasos esenciales hasta esteroides y lipoproteínas. Organizado de forma clara y visual, presenta cada categoría con sus estructuras, funciones y ejemplos clínicos.
Quimica organica
Guia con ejercicios quimica
Contenidos más populares
9Biologia
Fases
Conceptos Clave de la Revolución Industrial
Explora los términos esenciales de la Revolución Industrial, sus clases sociales y la urbanización.
Países y Capitales de América
Aprende los países y capitales de América del Sur, Central, Caribe y del Norte.
matematicas
ecuaciones
celula eucriota, membrana plasmática, núcleo, pared celular, citoplasma y citoesqueletos. nombre se las partes de la celula eucariota
Este quiz evalúa tu conocimiento sobre la célula eucariota, incluyendo la membrana plasmática, núcleo, pared celular, citoplasma y citoesqueleto.
Precalculo
Estoy estudiando temas de Álgebra y Trigonometría (logaritmos, funciones cuadráticas, identidades trigonométricas) y Física (vectores, cinemática, estática). Mi objetivo es aprobar el examen de ingreso a Ingeniería Industrial.
Análisis sintáctico de oraciones
explicación de el análisis de oraciones
Función cuadrática: Fórmulas y Análisis de la parábola.
Resumen teórico-práctico sobre la función cuadrática, sus fórmulas principales y el estudio de la parábola como representación gráfica.Incluye desarrollo de la forma general, cálculo de raíces, vértice y elementos fundamentales para su interpretación
Geografía 1er año
definición geografía-coordenadas geográficas-meridianos-paralelos-definición latitud y longitud-elementos del mapa-definición mapa-localización relativa y absoluta
¿No encuentras lo que buscas? Explora otros temas.
Mira lo que dicen nuestros usuarios. Les encantó — y a ti también te encantará.
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.