La configuración electrónica describe cómo se distribuyen los electrones de... Mostrar más
Inscríbete para ver los apuntes¡Es gratis!
Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Asignaturas
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostrar todos los temas
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostrar todos los temas
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostrar todos los temas
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostrar todos los temas
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostrar todos los temas
107
•
Actualizado Apr 14, 2026
•
Sofia Pelatti
@sofiapela_85n6o
La configuración electrónica describe cómo se distribuyen los electrones de... Mostrar más




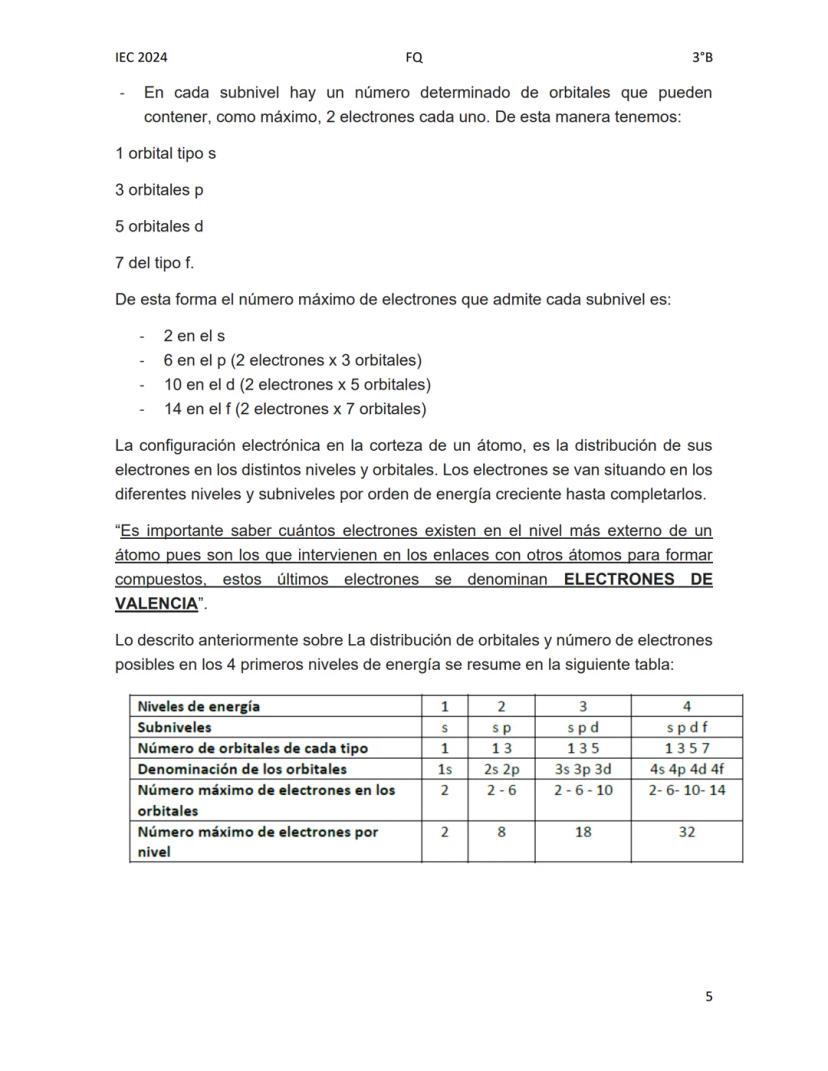

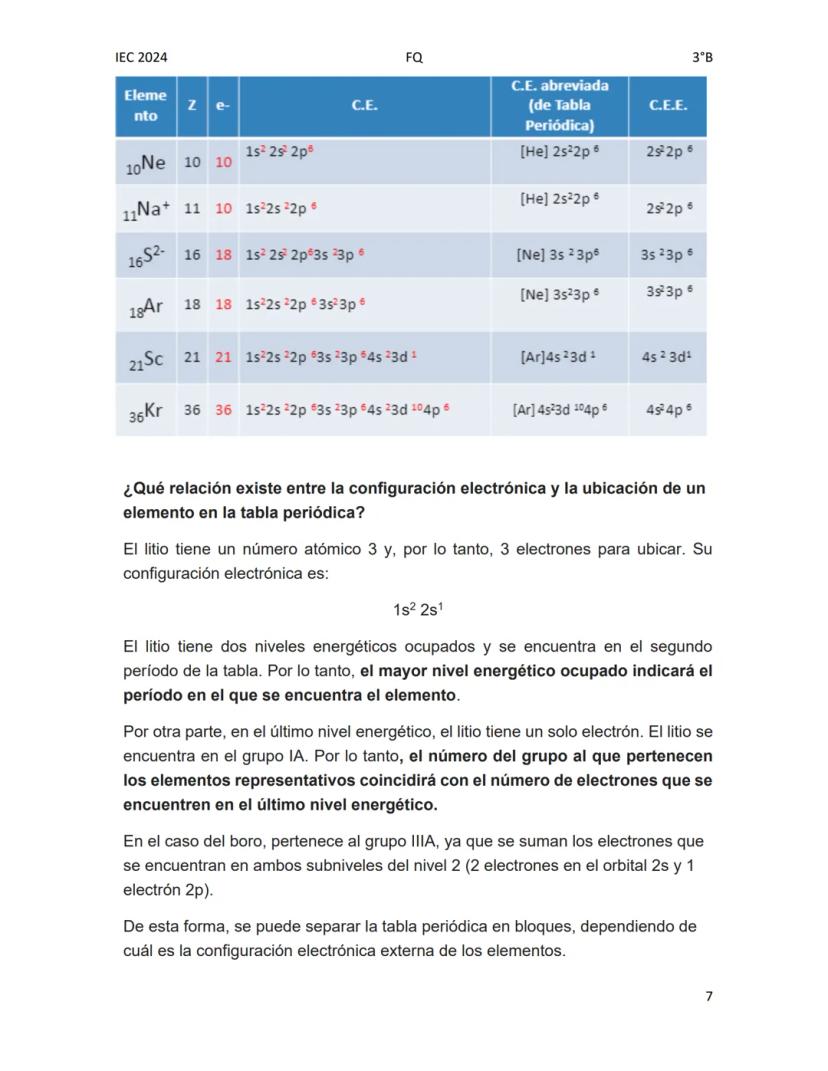

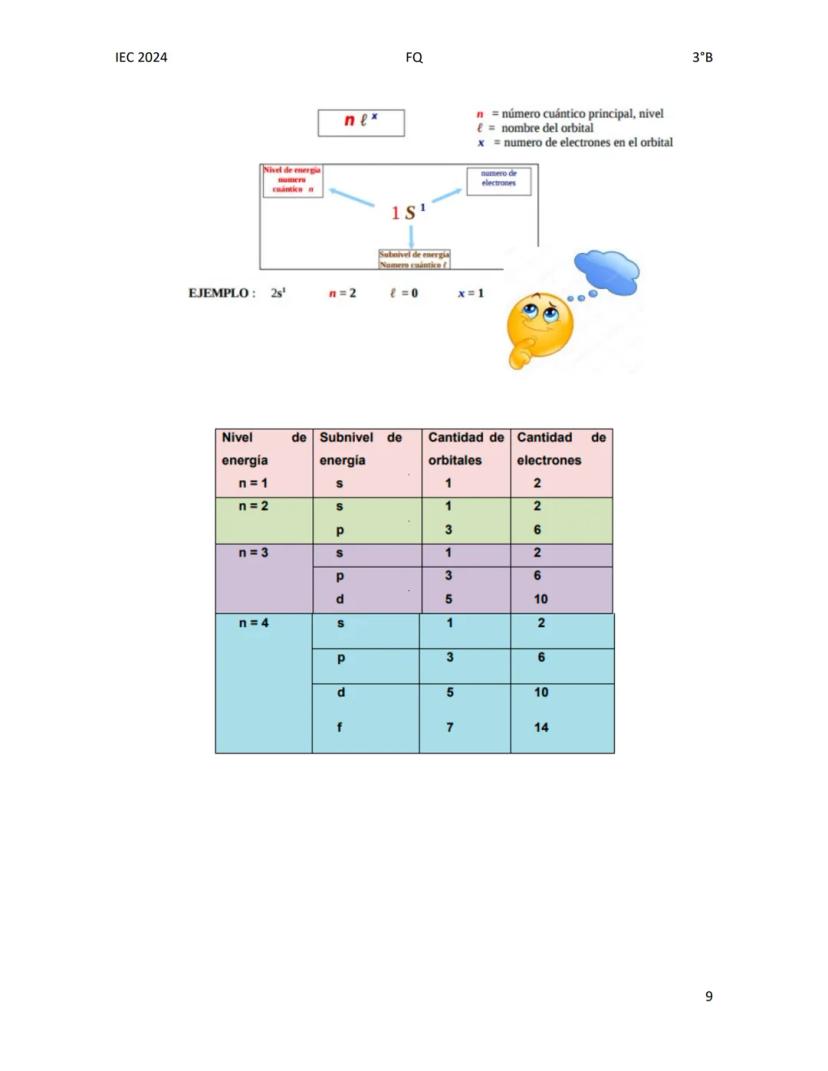



La configuración electrónica muestra cómo los electrones se distribuyen en los diferentes niveles y subniveles de energía de un átomo. Esta distribución sigue el principio de mínima energía, lo que significa que los electrones ocupan primero los niveles de menor energía.
Para escribir la configuración electrónica de un elemento, necesitas conocer su número atómico (Z), que indica cuántos electrones tiene. Por ejemplo, el hidrógeno tiene un solo electrón que se ubica en el orbital 1s, por lo que su configuración se escribe como 1s¹.
Los electrones se pueden representar gráficamente con flechas dentro de orbitales (↑↓), donde las direcciones opuestas indican electrones con spines opuestos. En un mismo orbital pueden ubicarse como máximo dos electrones, siempre con spines diferentes.
💡 La configuración electrónica no solo nos ayuda a entender la estructura atómica, sino que también explica por qué ciertos elementos reaccionan de manera similar o por qué algunos, como los gases nobles, son tan estables y no reaccionan.

Al distribuir electrones en los orbitales, debemos seguir tres principios fundamentales:
Principio de Aufbau: los electrones ocupan primero los orbitales de menor energía y luego los de mayor energía. La energía de los niveles aumenta en este orden: 1s, 2s, 2p, 3s, 3p, 4s, 3d...
Principio de exclusión de Pauli: en un mismo orbital sólo pueden existir dos electrones con spines opuestos. No pueden existir dos electrones con los mismos cuatro números cuánticos.
Regla de Hund: cuando hay varios orbitales de igual energía (como los orbitales p), los electrones se distribuyen uno en cada orbital con el mismo spin antes de empezar a aparearse.
La distancia energética entre niveles disminuye conforme nos alejamos del núcleo. Por eso, a veces un subnivel de un nivel superior (como el 4s) tiene menor energía que otro de un nivel inferior (como el 3d). Para recordar el orden correcto de llenado podemos usar el diagrama de Möller que sigue un patrón de diagonales.
¡No te preocupes si esto parece complicado! Con práctica podrás predecir fácilmente cómo se distribuyen los electrones en cualquier átomo.

El diagrama de Möller es una herramienta super útil para recordar el orden en que se llenan los orbitales. Se organiza siguiendo diagonales desde arriba hacia abajo, comenzando con 1s y siguiendo la flecha:
1s ←
2s ← 2p
3s 3p 3d
4s 4p 4d 4f
5s 5p 5d 5f
6s 6p 6d 6f
7s 7p 7d 7f
Siguiendo este patrón, el orden completo sería: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s² 4d¹⁰ 5p⁶ 6s² 4f¹⁴ 5d¹⁰ 6p⁶ 7s² 5f¹⁴ 6d¹⁰ 7p⁶
Para escribir la configuración electrónica de cualquier átomo, necesitás:
💡 ¿Sabías que puedes predecir las propiedades químicas de un elemento con solo mirar su configuración electrónica? Los elementos del mismo grupo tienen configuraciones similares en su última capa, ¡por eso reaccionan de manera parecida!

Al escribir configuraciones electrónicas, debés aplicar correctamente los tres principios fundamentales:
Mínima energía de Aufbau: los electrones siempre ocupan primero los orbitales de menor energía.
Principio de exclusión de Pauli: en cada orbital caben máximo dos electrones con spines opuestos. Es imposible que dos electrones tengan los mismos cuatro números cuánticos.
Principio de máxima multiplicidad de Hund: en orbitales de igual energía, los electrones entran de a uno, manteniendo el mismo spin. Solo después de ocupar todos los orbitales disponibles, comienzan a aparearse.
Por ejemplo, para el carbono con configuración 1s² 2s² 2p², hay tres posibles maneras de ubicar los electrones en el subnivel 2p:
2px 2py 2pz 2px 2py 2pz 2px 2py 2pz
↑↓ ↑ ↑ ↑↑
Sin embargo, solo la del medio cumple con la regla de Hund, ya que los electrones ocupan primero orbitales diferentes con el mismo spin.
Recuerda que cada nivel energético tiene diferentes subniveles (s, p, d, f) y cada subnivel tiene un número específico de orbitales que pueden contener máximo 2 electrones cada uno.
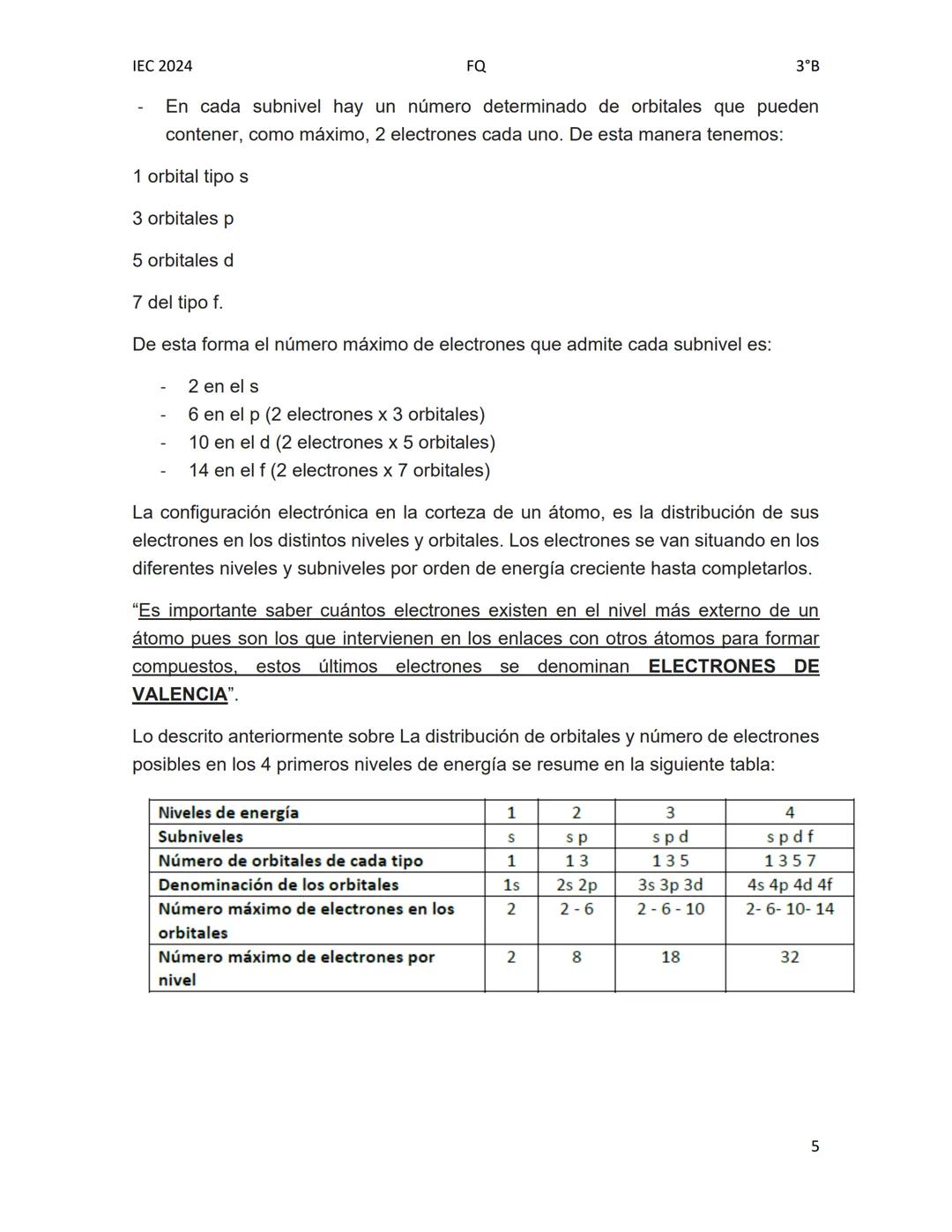
Los electrones se organizan en niveles y subniveles siguiendo un patrón específico. Es importante entender esta estructura:
La tabla siguiente muestra la distribución en los 4 primeros niveles:
| Nivel | Subniveles | Número máximo de electrones |
|---|---|---|
| 1 | s | 2 |
| 2 | s, p | 8 (2+6) |
| 3 | s, p, d | 18 (2+6+10) |
| 4 | s, p, d, f | 32 (2+6+10+14) |
💡 Los electrones de valencia son aquellos ubicados en el nivel más externo del átomo. Estos son los que participan en enlaces químicos y determinan las propiedades químicas del elemento. ¡Por eso son tan importantes!

Existen varias formas de escribir la configuración electrónica de un átomo:
La configuración electrónica externa (CEE) representa solo los electrones de la capa de valencia, que son los que determinan las propiedades químicas del elemento. Para encontrarla:
Por ejemplo:
La configuración electrónica externa es clave para entender el comportamiento químico de los elementos y por qué forman ciertos compuestos.
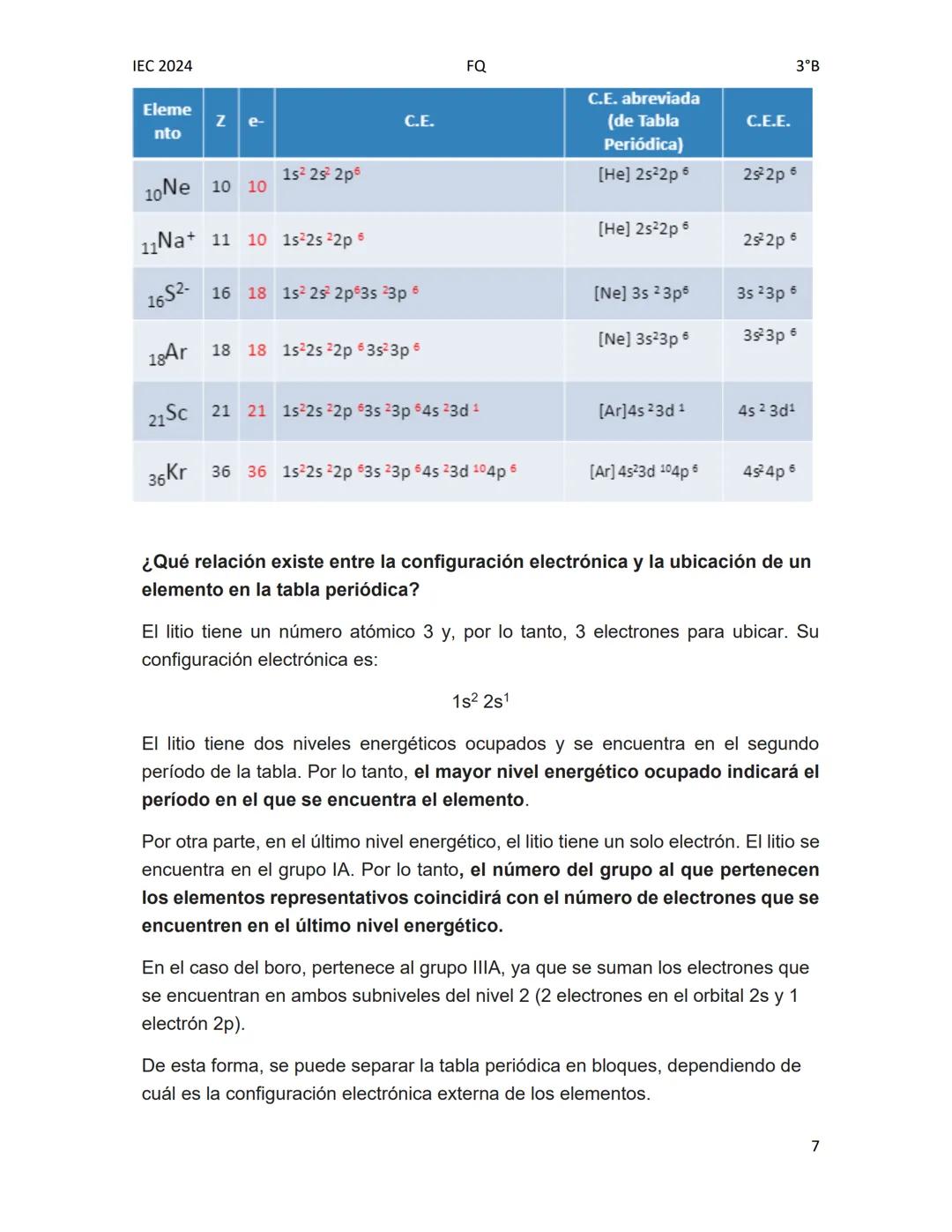
La configuración electrónica está directamente relacionada con la posición de un elemento en la tabla periódica. Esta relación nos permite predecir propiedades químicas:
El período (fila) corresponde al mayor nivel de energía ocupado. Por ejemplo, el litio (1s² 2s¹) tiene electrones hasta el nivel 2, por lo tanto está en el período 2.
Para los elementos representativos, el grupo (columna) corresponde al número de electrones en el último nivel. El litio tiene 1 electrón en su último nivel (2s¹), por eso está en el grupo IA.
La tabla periódica se organiza en bloques según el último subnivel que se llena:
Por ejemplo:
💡 Los gases nobles tienen configuraciones electrónicas muy estables con su último nivel completo (ns² np⁶), lo que explica por qué son tan poco reactivos.

La tabla periódica se divide en cuatro bloques según el último subnivel que se llena:
Bloque s: 2 elementos por nivel
Bloque p: 6 elementos por nivel
Bloque d: 10 elementos por nivel
Bloque f: 14 elementos por nivel
Las configuraciones más estables son aquellas donde:
Esto explica por qué los gases nobles son tan estables: tienen sus niveles de energía externos completos.
Las propiedades químicas de un elemento están determinadas principalmente por los electrones en su último nivel energético (electrones de valencia), ya que son los que participan en reacciones químicas y formación de enlaces.
Cuando escribimos la configuración electrónica, cada orbital se representa como: n^(e)l donde:
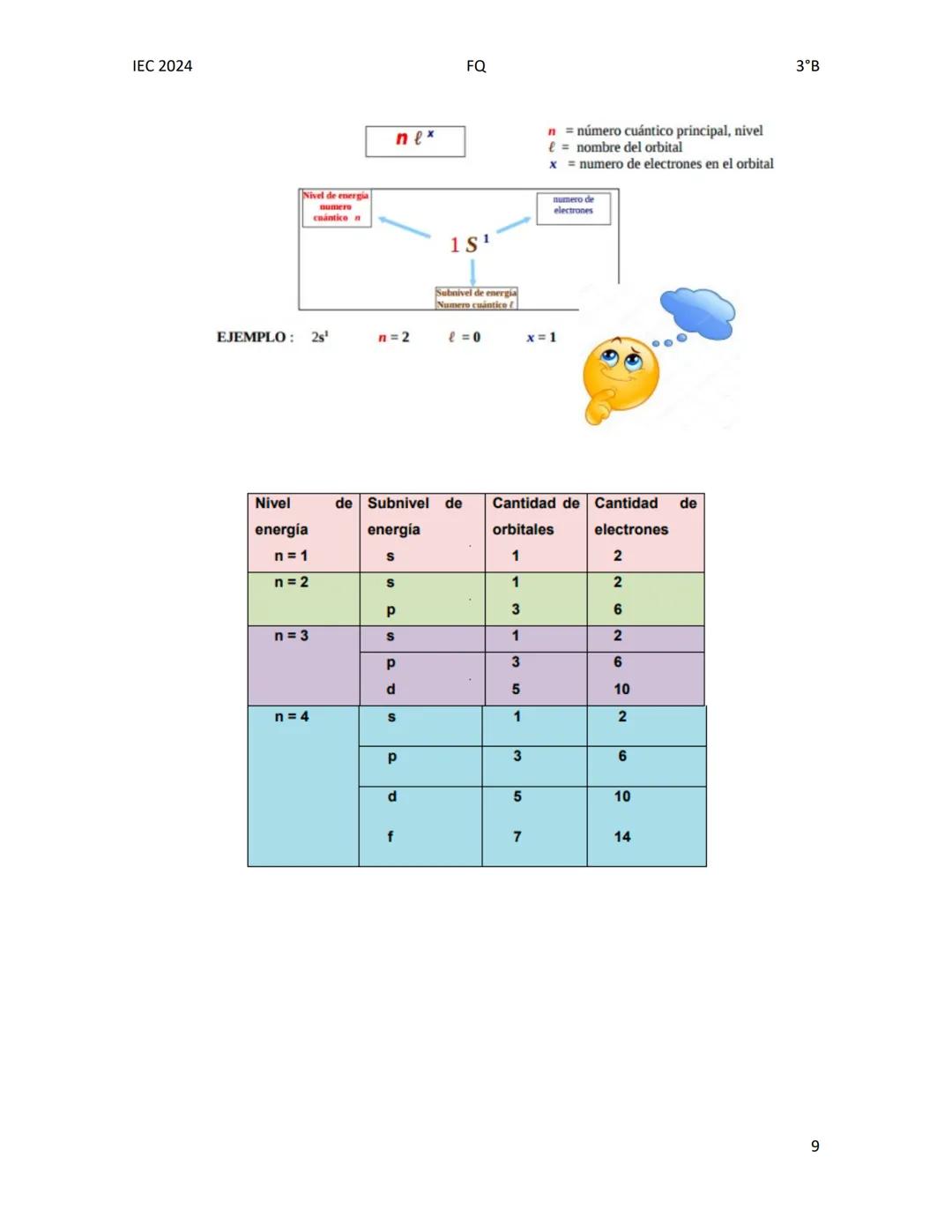
La configuración electrónica se basa en cuatro números cuánticos que describen completamente el estado de cada electrón:
Número cuántico principal (n): indica el nivel de energía y toma valores enteros positivos (1, 2, 3...)
Número cuántico secundario (l): determina la forma del orbital y puede tomar valores desde 0 hasta n-1
Número cuántico magnético (m): indica la orientación del orbital en el espacio y toma valores desde -l hasta +l
Número cuántico de spin (s): representa el giro del electrón sobre su propio eje y puede ser +½ o -½
Esta tabla muestra la relación entre niveles, subniveles, orbitales y número de electrones:
| Nivel | Subnivel | Orbitales (valores de m) | Máx. electrones |
|---|---|---|---|
| n=1 | s (l=0) | m=0 (1 orbital) | 2 |
| n=2 | s (l=0) | m=0 (1 orbital) | 2 |
| p (l=1) | m=-1,0,+1 (3 orbitales) | 6 | |
| n=3 | s (l=0) | m=0 (1 orbital) | 2 |
| p (l=1) | m=-1,0,+1 (3 orbitales) | 6 | |
| d (l=2) | m=-2,-1,0,+1,+2 (5 orbs) | 10 |
💡 Cada nivel n puede contener como máximo 2n² electrones. Por ejemplo, el nivel n=2 puede contener hasta 2(2)² = 8 electrones.

La forma más visual de representar los electrones es mediante diagramas de orbitales. Cada orbital se dibuja como un pequeño cuadrado que puede contener hasta dos electrones (representados por flechas):
Las flechas en sentido contrario indican que los electrones tienen spines opuestos.
Veamos algunos ejemplos:
| Átomo | Z | Configuración electrónica | Representación |
|---|---|---|---|
| Li | 3 | 1s² 2s¹ | ↑↓ ↑ |
| Be | 4 | 1s² 2s² | ↑↓ ↑↓ |
| B | 5 | 1s² 2s² 2p¹ | ↑↓ ↑↓ ↑ |
| C | 6 | 1s² 2s² 2p² | ↑↓ ↑↓ ↑ ↑ |
Los cuatro números cuánticos describen completamente el estado de un electrón:
Estos números nos permiten identificar de forma única a cada electrón en el átomo, y ningún electrón puede tener los cuatro números idénticos (principio de exclusión de Pauli).
💡 Cuando resolvas ejercicios, recuerda siempre aplicar los tres principios fundamentales: Aufbau (orden de llenado), Pauli (máximo dos electrones por orbital) y Hund (electrones desapareados antes que apareados).

Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
Sofia Pelatti
@sofiapela_85n6o
La configuración electrónica describe cómo se distribuyen los electrones de un átomo alrededor del núcleo, determinando sus propiedades químicas y su comportamiento. Este concepto es fundamental para entender por qué los elementos reaccionan de cierta manera y por qué los... Mostrar más

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La configuración electrónica muestra cómo los electrones se distribuyen en los diferentes niveles y subniveles de energía de un átomo. Esta distribución sigue el principio de mínima energía, lo que significa que los electrones ocupan primero los niveles de menor energía.
Para escribir la configuración electrónica de un elemento, necesitas conocer su número atómico (Z), que indica cuántos electrones tiene. Por ejemplo, el hidrógeno tiene un solo electrón que se ubica en el orbital 1s, por lo que su configuración se escribe como 1s¹.
Los electrones se pueden representar gráficamente con flechas dentro de orbitales (↑↓), donde las direcciones opuestas indican electrones con spines opuestos. En un mismo orbital pueden ubicarse como máximo dos electrones, siempre con spines diferentes.
💡 La configuración electrónica no solo nos ayuda a entender la estructura atómica, sino que también explica por qué ciertos elementos reaccionan de manera similar o por qué algunos, como los gases nobles, son tan estables y no reaccionan.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Al distribuir electrones en los orbitales, debemos seguir tres principios fundamentales:
Principio de Aufbau: los electrones ocupan primero los orbitales de menor energía y luego los de mayor energía. La energía de los niveles aumenta en este orden: 1s, 2s, 2p, 3s, 3p, 4s, 3d...
Principio de exclusión de Pauli: en un mismo orbital sólo pueden existir dos electrones con spines opuestos. No pueden existir dos electrones con los mismos cuatro números cuánticos.
Regla de Hund: cuando hay varios orbitales de igual energía (como los orbitales p), los electrones se distribuyen uno en cada orbital con el mismo spin antes de empezar a aparearse.
La distancia energética entre niveles disminuye conforme nos alejamos del núcleo. Por eso, a veces un subnivel de un nivel superior (como el 4s) tiene menor energía que otro de un nivel inferior (como el 3d). Para recordar el orden correcto de llenado podemos usar el diagrama de Möller que sigue un patrón de diagonales.
¡No te preocupes si esto parece complicado! Con práctica podrás predecir fácilmente cómo se distribuyen los electrones en cualquier átomo.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
El diagrama de Möller es una herramienta super útil para recordar el orden en que se llenan los orbitales. Se organiza siguiendo diagonales desde arriba hacia abajo, comenzando con 1s y siguiendo la flecha:
1s ←
2s ← 2p
3s 3p 3d
4s 4p 4d 4f
5s 5p 5d 5f
6s 6p 6d 6f
7s 7p 7d 7f
Siguiendo este patrón, el orden completo sería: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s² 4d¹⁰ 5p⁶ 6s² 4f¹⁴ 5d¹⁰ 6p⁶ 7s² 5f¹⁴ 6d¹⁰ 7p⁶
Para escribir la configuración electrónica de cualquier átomo, necesitás:
💡 ¿Sabías que puedes predecir las propiedades químicas de un elemento con solo mirar su configuración electrónica? Los elementos del mismo grupo tienen configuraciones similares en su última capa, ¡por eso reaccionan de manera parecida!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Al escribir configuraciones electrónicas, debés aplicar correctamente los tres principios fundamentales:
Mínima energía de Aufbau: los electrones siempre ocupan primero los orbitales de menor energía.
Principio de exclusión de Pauli: en cada orbital caben máximo dos electrones con spines opuestos. Es imposible que dos electrones tengan los mismos cuatro números cuánticos.
Principio de máxima multiplicidad de Hund: en orbitales de igual energía, los electrones entran de a uno, manteniendo el mismo spin. Solo después de ocupar todos los orbitales disponibles, comienzan a aparearse.
Por ejemplo, para el carbono con configuración 1s² 2s² 2p², hay tres posibles maneras de ubicar los electrones en el subnivel 2p:
2px 2py 2pz 2px 2py 2pz 2px 2py 2pz
↑↓ ↑ ↑ ↑↑
Sin embargo, solo la del medio cumple con la regla de Hund, ya que los electrones ocupan primero orbitales diferentes con el mismo spin.
Recuerda que cada nivel energético tiene diferentes subniveles (s, p, d, f) y cada subnivel tiene un número específico de orbitales que pueden contener máximo 2 electrones cada uno.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Los electrones se organizan en niveles y subniveles siguiendo un patrón específico. Es importante entender esta estructura:
La tabla siguiente muestra la distribución en los 4 primeros niveles:
| Nivel | Subniveles | Número máximo de electrones |
|---|---|---|
| 1 | s | 2 |
| 2 | s, p | 8 (2+6) |
| 3 | s, p, d | 18 (2+6+10) |
| 4 | s, p, d, f | 32 (2+6+10+14) |
💡 Los electrones de valencia son aquellos ubicados en el nivel más externo del átomo. Estos son los que participan en enlaces químicos y determinan las propiedades químicas del elemento. ¡Por eso son tan importantes!

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Existen varias formas de escribir la configuración electrónica de un átomo:
La configuración electrónica externa (CEE) representa solo los electrones de la capa de valencia, que son los que determinan las propiedades químicas del elemento. Para encontrarla:
Por ejemplo:
La configuración electrónica externa es clave para entender el comportamiento químico de los elementos y por qué forman ciertos compuestos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La configuración electrónica está directamente relacionada con la posición de un elemento en la tabla periódica. Esta relación nos permite predecir propiedades químicas:
El período (fila) corresponde al mayor nivel de energía ocupado. Por ejemplo, el litio (1s² 2s¹) tiene electrones hasta el nivel 2, por lo tanto está en el período 2.
Para los elementos representativos, el grupo (columna) corresponde al número de electrones en el último nivel. El litio tiene 1 electrón en su último nivel (2s¹), por eso está en el grupo IA.
La tabla periódica se organiza en bloques según el último subnivel que se llena:
Por ejemplo:
💡 Los gases nobles tienen configuraciones electrónicas muy estables con su último nivel completo (ns² np⁶), lo que explica por qué son tan poco reactivos.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La tabla periódica se divide en cuatro bloques según el último subnivel que se llena:
Bloque s: 2 elementos por nivel
Bloque p: 6 elementos por nivel
Bloque d: 10 elementos por nivel
Bloque f: 14 elementos por nivel
Las configuraciones más estables son aquellas donde:
Esto explica por qué los gases nobles son tan estables: tienen sus niveles de energía externos completos.
Las propiedades químicas de un elemento están determinadas principalmente por los electrones en su último nivel energético (electrones de valencia), ya que son los que participan en reacciones químicas y formación de enlaces.
Cuando escribimos la configuración electrónica, cada orbital se representa como: n^(e)l donde:

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La configuración electrónica se basa en cuatro números cuánticos que describen completamente el estado de cada electrón:
Número cuántico principal (n): indica el nivel de energía y toma valores enteros positivos (1, 2, 3...)
Número cuántico secundario (l): determina la forma del orbital y puede tomar valores desde 0 hasta n-1
Número cuántico magnético (m): indica la orientación del orbital en el espacio y toma valores desde -l hasta +l
Número cuántico de spin (s): representa el giro del electrón sobre su propio eje y puede ser +½ o -½
Esta tabla muestra la relación entre niveles, subniveles, orbitales y número de electrones:
| Nivel | Subnivel | Orbitales (valores de m) | Máx. electrones |
|---|---|---|---|
| n=1 | s (l=0) | m=0 (1 orbital) | 2 |
| n=2 | s (l=0) | m=0 (1 orbital) | 2 |
| p (l=1) | m=-1,0,+1 (3 orbitales) | 6 | |
| n=3 | s (l=0) | m=0 (1 orbital) | 2 |
| p (l=1) | m=-1,0,+1 (3 orbitales) | 6 | |
| d (l=2) | m=-2,-1,0,+1,+2 (5 orbs) | 10 |
💡 Cada nivel n puede contener como máximo 2n² electrones. Por ejemplo, el nivel n=2 puede contener hasta 2(2)² = 8 electrones.

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
La forma más visual de representar los electrones es mediante diagramas de orbitales. Cada orbital se dibuja como un pequeño cuadrado que puede contener hasta dos electrones (representados por flechas):
Las flechas en sentido contrario indican que los electrones tienen spines opuestos.
Veamos algunos ejemplos:
| Átomo | Z | Configuración electrónica | Representación |
|---|---|---|---|
| Li | 3 | 1s² 2s¹ | ↑↓ ↑ |
| Be | 4 | 1s² 2s² | ↑↓ ↑↓ |
| B | 5 | 1s² 2s² 2p¹ | ↑↓ ↑↓ ↑ |
| C | 6 | 1s² 2s² 2p² | ↑↓ ↑↓ ↑ ↑ |
Los cuatro números cuánticos describen completamente el estado de un electrón:
Estos números nos permiten identificar de forma única a cada electrón en el átomo, y ningún electrón puede tener los cuatro números idénticos (principio de exclusión de Pauli).
💡 Cuando resolvas ejercicios, recuerda siempre aplicar los tres principios fundamentales: Aufbau (orden de llenado), Pauli (máximo dos electrones por orbital) y Hund (electrones desapareados antes que apareados).

Acceso a todos los documentos
Mejora tus notas
Únete a millones de estudiantes
Nuestro compañero de IA está específicamente adaptado a las necesidades de los estudiantes. Basándonos en los millones de contenidos que tenemos en la plataforma, podemos dar a los estudiantes respuestas realmente significativas y relevantes. Pero no se trata solo de respuestas, el compañero también guía a los estudiantes a través de sus retos de aprendizaje diarios, con planes de aprendizaje personalizados, cuestionarios o contenidos en el chat y una personalización del 100% basada en las habilidades y el desarrollo de los estudiantes.
Puedes descargar la app en Google Play Store y Apple App Store.
¡Sí lo es! Tienes acceso totalmente gratuito a todo el contenido de la app, puedes chatear con otros alumnos y recibir ayuda inmeditamente. Puedes ganar dinero utilizando la aplicación, que te permitirá acceder a determinadas funciones.
1
Herramientas Inteligentes NUEVO
Transformá estos apuntes en: ✓ 50+ Preguntas de Práctica ✓ Fichas Interactivas ✓ Simulacro Completo de Examen ✓ Esquemas de Ensayo
App Store
Google Play
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia
La app es muy fácil de usar y está muy bien diseñada. Hasta ahora he encontrado todo lo que estaba buscando y he podido aprender mucho de las presentaciones. Definitivamente utilizaré la aplicación para un examen de clase. Y, por supuesto, también me sirve mucho de inspiración.
Pablo
usuario de iOS
Esta app es realmente genial. Hay tantos apuntes de clase y ayuda [...]. Tengo problemas con matemáticas, por ejemplo, y la aplicación tiene muchas opciones de ayuda. Gracias a Knowunity, he mejorado en mates. Se la recomiendo a todo el mundo.
Elena
usuaria de Android
Vaya, estoy realmente sorprendida. Acabo de probar la app porque la he visto anunciada muchas veces y me he quedado absolutamente alucinada. Esta app es LA AYUDA que quieres para el insti y, sobre todo, ofrece muchísimas cosas, como ejercicios y hojas informativas, que a mí personalmente me han sido MUY útiles.
Ana
usuaria de iOS
Una increíble aplicación, de verdad. Apareció en el momento en que necesitaba una app que me ayude a organizar mis estudios, al igual que para prepararme para los exámenes. Te da una increíble variedad de estudio que simplemente me encanta. Además de ser una gran ayuda para estudiantes de diferentes grados, como la universidad, lo que más me gusta de esta app es que está para diferentes países.
Bárbara
Chile
Me encantó. La app es superior, buena para los estudiantes. No solo te da las respuestas, sino que también te las explica de una manera asombrosa, lo que hace que entiendas súper rápido. La recomiendo mucho si se te hace difícil comprender las materias que te dejan.
Jennifer
Perú
Muy buena aplicación, da información precisa de lo que se le pide. Es eficiente y, sobre todo, tiene varios intereses a escoger, como por ejemplo, temas sobre el ICFES, temas de bachillerato, entre otros. Excelente app.
Lady
Colombia
¡La app es buenísima! Sólo tengo que introducir el tema en la barra de búsqueda y recibo la respuesta muy rápido. No tengo que ver 10 vídeos de YouTube para entender algo, así que me ahorro tiempo. ¡Muy recomendable!
Sara
usuaria de Android
En el instituto era muy malo en matemáticas, pero gracias a la app, ahora saco mejores notas. Os agradezco mucho que hayáis creado la aplicación.
Roberto
usuario de Android
Me costaba demasiado estudiar porque no entiendo cuando me pongo a estudiar, y en los exámenes me iba mal, hasta que me empezaron a aparecer anuncios y la descargué sin tenerle fe. Gracias a esta aplicación, algo que no entendía hace meses y semanas lo entendí. En esta aplicación mis notas mejoraron, y ya no me tengo que preocupar por estudiar.
Antonella
Argentina
¡Excelente! Amé la app. Me parece súper eficiente. Aparte de que enseña mucho, te ayuda en tus problemas personales y te hace resúmenes. Amo. Amé un montón la app. Sirve para cualquier año, desde sexto hasta quinto año. Aparte, hay resúmenes de otras personas. ¡Nonono, loquísimo! Te la recomiendo al 100%. Efectivamente, es un 10/10.
Usuario argentino
iOS.
Excelente experiencia. La aplicación es buenísima, la recomiendo mucho. Es mucho mejor que ChatGPT. Te manda la respuesta de tus búsquedas y, aparte, diapositivas para estudiar. Es magnífica.
Alo
México
¡ME ENCANTA! Todo es muy sencillo de utilizar y aprender. Mi IA es muy buena y los apuntes de los demás estudiantes son súper buenos; explica las cosas súper bien y detalladamente. La amo. Pruébenla.
Kitty
Colombia